��Ŀ����
���������Ȼ�ѧ����ʽ�ó��Ľ�����ȷ����
A����֪��C(ʯī��s)==C(���ʯ��s)  ������ʯ��ʯī�ȶ�
������ʯ��ʯī�ȶ�
B����֪:2H2(g)+O2(g)==2H2O(g)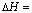 -483.6kJ��mol-1����������ȼ����Ϊ241.8kJ��mol-1
-483.6kJ��mol-1����������ȼ����Ϊ241.8kJ��mol-1
C�� ��֪��500�桢30MPa�£�N2(g)+3H2(g)  2NH3 (g)
2NH3 (g) 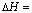 -38.6kJ��mol-1����1.5molH2������N2�ڴ������³�ַ�Ӧ���ų�����19.3kJ
-38.6kJ��mol-1����1.5molH2������N2�ڴ������³�ַ�Ӧ���ų�����19.3kJ
D�� ��֪�� H2(g)+F2(g)== 2HF(g) 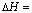 -270kJ��mol-1������ͬ�����£�2molHF���������С��1mol������1mol����������֮��
-270kJ��mol-1������ͬ�����£�2molHF���������С��1mol������1mol����������֮��
D

�����Ϊ2 L���ܱ������У��������»�ѧ��Ӧ��
CO2(g)��H2(g) CO(g)��H2O(g) ��H=Q����ѧƽ�ⳣ��K���¶�T�Ĺ�ϵ���±���
CO(g)��H2O(g) ��H=Q����ѧƽ�ⳣ��K���¶�T�Ĺ�ϵ���±���
| T/�� | 700 | 800 | 850 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
�ش��������⣺
��1��Q____0���� ��>������<�����������¶ȣ���ѧƽ����________(�����Ӧ�����淴Ӧ��)�����ƶ���
��2����ij�¶��£�ƽ��Ũ�ȷ������й�ϵ��c(CO2)��c(H2)��c(CO)��c(H2O)����ʱ���¶�Ϊ__________���ڴ��¶��£����������к���1mol CO2��3mol H2��2mol CO��2mol H2O�����ʱ��Ӧ������״̬Ϊ____________(�������Ӧ��������С��������淴Ӧ��������С���ƽ��״̬��)�����¶�ƽ��ʱCO2��Ũ��Ϊ___________ mol��L��1���ڴ��¶��£����������к���1.5mol CO2��3.5mol H2��1.5mol CO��1.5mol H2O�ﵽƽ��ʱCO2��Ũ��Ϊ___________ mol��L��1��
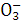 ��Na+
��Na+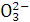 ��Cl-��F-��K+
��Cl-��F-��K+
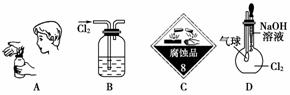
 ����˵����ȷ����( )
����˵����ȷ����( )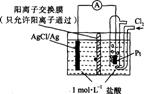 A��������ӦΪ
A��������ӦΪ