题目内容
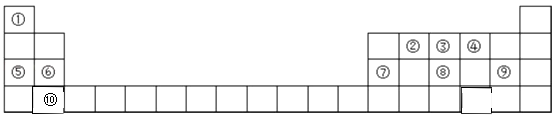
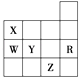
【题目】A、B、C、D、E、X均为短周期元素形成的无机物,存在下图所示转化关系(部分生成物和反应条件略去);已知A由短周期非金属元素组成,B具有漂白性且光照易分解。请回答以下问题:

(1)若A为单质,且C为一元强酸。
①组成单质A的元素在元素周期表中的位置为__________。
②写出一种工业制备单质A方法的离子方程式: __________。
③X可能为________(填字母代号)。
a.NaOH b. AlCl3 c.Na2CO3 d.NaAlO2
(2)若A为两种元素形成的化合物,且E与水反应生成的G的浓溶液遇C有白烟产生。
①A的电子式为__________。
②A与H2O反应的化学方程式为__________。
③G的浓溶液遇C产生白烟的化学方程式为__________。
【答案】 第三周期第ⅦA族 2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑(或2Na++2Cl-
2OH-+H2↑+Cl2↑(或2Na++2Cl-![]() 2Na+Cl2↑等其他合理答案均可) cd
2Na+Cl2↑等其他合理答案均可) cd  NCl3+3H2O=3HClO+NH3 HNO3+NH3=NH4NO3
NCl3+3H2O=3HClO+NH3 HNO3+NH3=NH4NO3
【解析】本题主要考查氯化氢、氯化钠等氯的化合物的性质。
B具有漂白性且光照易分解,据此可知B是次氯酸。
(1)若A为单质,且C为一元强酸,由于氯气与水反应产生盐酸与次氯酸,则A为氯气。
①组成单质A的元素氯元素在元素周期表中的位置为第三周期第VIIA族。
②工业制备单质A方法的离子方程式:2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑(或2Na++2Cl-
2OH-+H2↑+Cl2↑(或2Na++2Cl-![]() 2Na+Cl2↑等其他合理答案均可)。
2Na+Cl2↑等其他合理答案均可)。
③C为盐酸。a.NaOH与盐酸反应生成NaCl,NaCl与NaOH不反应,故a不符合题意;b. AlCl3与盐酸不反应,故b不符合题意;c.Na2CO3与盐酸反应生成CO2,CO2与Na2CO3及H2O反应生成NaHCO3,故c符合题意;d.NaAlO2与盐酸反应生成AlCl3,AlCl3与NaAlO2反应生成Al(OH)3,故d符合题意。故选cd。
(2)若A 为两种元素形成的化合物,且E 与水反应生成的G的浓溶液遇C 有白烟产生,则A为NCl3,白烟成分为硝酸铵。
①A的电子式为![]() 。
。
②A与H2O反应的化学方程式为NCl3+3H2O=3HClO+NH3。
③G的浓溶液遇C产生白烟的化学方程式为HNO3+NH3=NH4NO3。