题目内容
下列关于二氧化硫性质的说法正确的是
| A.氯水中通入一定量二氧化硫气体可增强氯水的漂白性 |
| B.含有酚酞的氢氧化钠溶液中通入二氧化硫气体,溶液变无色,说明二氧化硫具有漂白性 |
| C.二氧化硫既可被氧化也可被还原 |
| D.紫色石蕊试液中通入二氧化硫,溶液先变红后退色 |
C
解析试题分析:A、氯水中通入一定量二氧化硫气体可降低氯水的漂白性,因为二者反应SO2+Cl2+2H2O=H2SO4+2HCl,A不正确;B、二氧化硫是酸性氧化物与氢氧化钠反应,因此含有酚酞的氢氧化钠溶液中通入二氧化硫气体,溶液变无色,二氧化硫具有漂白性但不能漂白酸碱指示剂,B不正确;C、二氧化硫中硫元素是+4价,处于中间价态,因此二氧化硫既可被氧化也可被还原,C正确;D、二氧化硫溶于水生成亚硫酸,所以紫色石蕊试液中通入二氧化硫,溶液变红色,但不能褪色,因为二氧化硫不能漂白酸碱指示剂,D不正确,答案选C。
考点:考查二氧化硫性质的正误判断

 名师点拨卷系列答案
名师点拨卷系列答案下列微粒的存在最能说明碘可能呈现金属性的是
| A.IBr | B.I2O5 | C.I3+ | D.I3- |
某研究性学习小组做铜与浓硫酸反应实验时,发现试管底部有白色固体甲并夹杂有少量黑色物质乙。倒去试管中的浓硫酸,将剩余固体(含少量浓硫酸)倒入盛有少量水的烧杯中,发现所得溶液为蓝色,仍有未溶解的黑色固体丙。过滤、洗涤后,向黑色固体丙中加入过量浓硝酸,黑色固体溶解,溶液呈蓝色,所得溶液加BaCl2溶液后有白色沉淀生成。下列所得结论不正确的是
| A.铜与浓硫酸反应所得白色固体甲是CuSO4 |
| B.加BaCl2溶液后所得白色沉淀是BaSO3 |
| C.白色固体甲中夹杂的少量黑色物质乙中可能含有CuO |
| D.白色固体甲中夹杂的少量黑色物质乙中含元素Cu、S |
水处理包括水的净化、杀菌消毒、蒸馏等。其中常见的杀菌消毒剂包括氯气、臭氧、漂白粉、活性炭等。游泳场馆往往用臭氧、活性炭对游泳池进行消毒和净化。下列说法中正确的是 ( )。
| A.臭氧、活性炭处理水的原理相同 |
| B.氯气是一种常用的消毒剂,用氯气消毒的水也可以用于配制化学试剂 |
| C.氯气和二氧化硫都具有漂白性,等体积的两者混合会提高漂白的效率 |
| D.漂白粉长期露置在空气中会失效 |
某同学用下列装置制备并检验Cl2的性质。下列说法正确的是 ( )。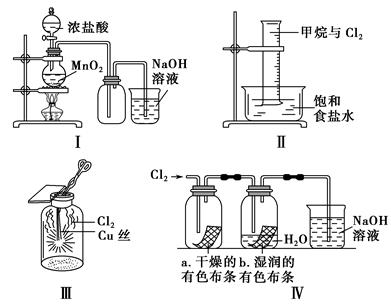
| A.Ⅰ图中:如果MnO2过量,浓盐酸就可被全部消耗 |
| B.Ⅱ图中:量筒中发生了加成反应 |
| C.Ⅲ图中:生成蓝色的烟 |
| D.Ⅳ图中:湿润的有色布条能退色,将硫酸溶液滴入烧杯中,至溶液显酸性,结果有Cl2生成 |
下列溶液中通入SO2一定不会产生沉淀的是( )
| A.Ba(OH)2 | B.Ba(NO3)2 | C.Na2S | D.BaCl2 |
下列有关物质的应用正确的是( )
| A.硅酸钙可用于生产黏合剂和防火剂 |
| B.用石英器皿盛放氢氟酸 |
| C.SiO2和CO2都能溶于水且与水反应生成相应的酸 |
| D.用NaHCO3治疗胃酸过多 |
氯气用途十分广泛,可用于生产半导体材料硅,其生产的流程如下,下列说法不正确的是( )
| A.①③是置换反应,②是化合反应 |
| B.高温下,焦炭与氢气的还原性均强于硅的 |
| C.任一反应中,每消耗或生成28 g硅,均转移4 mol电子 |
| D.高温下将石英砂、焦炭、氯气、氢气按一定比例混合可得高纯硅 |
(CN)2、(OCN)2、(SCN)2等物质的性质与卤素单质相似,而CN-、OCN-、SCN-等离子的性质与卤离子相似,化学上分别将其称之为类卤素和类卤离子,不同的卤素也可以生成卤素互化物,如BrF3。下列关于(CN)2的性质的叙述中,不像卤素的是( )
| A.能在空气中燃烧 |
| B.可与银、汞、铅等生成难溶盐 |
| C.在碱溶液中生成CN-和OCN- |
| D.与Cl2反应生成CNCl |