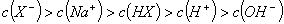题目内容
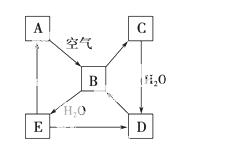
某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如右图所示。
(1)由图中所给数据进行分析,该反应的化学方程式为___________________________________;
(2)反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)=__________________。
Ⅱ(7分)将2mol H2O和2mol CO置于1L容器中,加热至高温,发生如下可逆反应:
2H2O(g)  2H2(g)+O2(g),2CO(g)+O2(g)
2H2(g)+O2(g),2CO(g)+O2(g)  2CO2(g)。
2CO2(g)。
(3)当上述系统达到平衡时,欲求混合气体的平衡组成,至少还需要知道两种气体的平衡浓度,但这两种气体不能同时是________和________,或________和________(填分子式)。
(4)若平衡时O2和CO2的物质的量分别为a mol和b mol,则平衡时H2O的物质的量为_______________________ (用含a、b的代数式表示)
Ⅰ(5分)(1)3X+Y 2Z (3分)
2Z (3分)
(2)0.05 mol·L-1·min-1(2分)
Ⅱ(7分)(3)H2O.H2,CO.CO2 (各1分)
(4)(2-2a-b)mol(3分)

练习册系列答案
相关题目
室温下,有关下列四种溶液的叙述正确的是(忽略溶液混合的体积变化)
| ① | ② | ③ | ④ | |
| pH | 12 | 12 | 2 | 2 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
A.在①、②中分别加入氯化铵晶体,两溶液的pH值均增大
B.分别将等体积的①和②加水稀释120倍,所得溶液的pH:①>②
C.把①、④两溶液等体积混合后所得溶液中:c(Cl-)>c(NH4+)>c(OH-)>c(H+)
D.将溶液②和溶液③等体积混合,混合后所得溶液pH=7
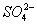 B. Al3+、Na+、
B. Al3+、Na+、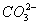 、
、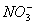
 2C(g),下列说法中正确的是
2C(g),下列说法中正确的是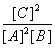
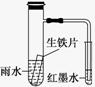
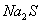 和
和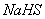 混合溶液中:
混合溶液中: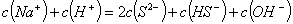
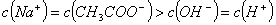
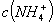 相等的①
相等的①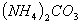 、②
、②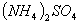 、③
、③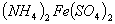 三种溶液中,溶质的物质的量浓度大小:①>②>③
三种溶液中,溶质的物质的量浓度大小:①>②>③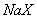 和弱酸
和弱酸 混合后呈酸性的溶液中:
混合后呈酸性的溶液中: