题目内容
(2012?江苏)利用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化尾气,又能获得应用广泛的Ca(NO2)2,其部分工艺流程如下:

(1)一定条件下,NO 与NO2 存在下列反应:NO(g)+NO2(g)?N2O3(g),其平衡常数表达式为K=
.
(2)上述工艺中采用气-液逆流接触吸收(尾气从吸收塔底进入,石灰乳从吸收塔顶喷淋),其目的是
(3)该工艺需控制NO 和NO2 物质的量之比接近1 颐1.若n(NO):n(NO2)>1 颐1,则会导致
(4)生产中溶液需保持弱碱性,在酸性溶液中Ca(NO2)2 会发生分解,产物之一是NO,其反应的离子方程式为

(1)一定条件下,NO 与NO2 存在下列反应:NO(g)+NO2(g)?N2O3(g),其平衡常数表达式为K=
| c(N2O3) |
| c(NO)?c(NO2) |
| c(N2O3) |
| c(NO)?c(NO2) |
(2)上述工艺中采用气-液逆流接触吸收(尾气从吸收塔底进入,石灰乳从吸收塔顶喷淋),其目的是
使尾气中NO、NO2被充分吸收
使尾气中NO、NO2被充分吸收
;滤渣可循环使用,滤渣的主要成分是Ca(OH)2
Ca(OH)2
(填化学式).(3)该工艺需控制NO 和NO2 物质的量之比接近1 颐1.若n(NO):n(NO2)>1 颐1,则会导致
排放气体中NO含量升高
排放气体中NO含量升高
;若n(NO):n(NO2)<1 颐1,则会导致产品Ca(NO2)2中Ca(NO3)2含量升高
产品Ca(NO2)2中Ca(NO3)2含量升高
.(4)生产中溶液需保持弱碱性,在酸性溶液中Ca(NO2)2 会发生分解,产物之一是NO,其反应的离子方程式为
3NO2-+2H+=NO3-+2NO↑+H2O
3NO2-+2H+=NO3-+2NO↑+H2O
.分析:(1)化学平衡常数,是指在一定温度下,可逆反应达到平衡时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值;
(2)使尾气中NO、NO2与石灰乳充分接触;滤渣的主要成分是Ca(OH)2;
(3)若n(NO):n(NO2)>1:1,则一氧化氮过量,若<1:1,则二氧化氮过量;
(4)根据质量守恒和电荷守恒定律书写;
(2)使尾气中NO、NO2与石灰乳充分接触;滤渣的主要成分是Ca(OH)2;
(3)若n(NO):n(NO2)>1:1,则一氧化氮过量,若<1:1,则二氧化氮过量;
(4)根据质量守恒和电荷守恒定律书写;
解答:解:(1)化学平衡常数,是指在一定温度下,可逆反应达到平衡时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,NO(g)+NO2(g)?N2O3(g),其平衡常数表达式为K=
,故答案为:
;
(2)使尾气中NO、NO2与石灰乳充分接触,NO、NO2被充分吸收;滤渣主要成分是Ca(OH)2,故答案为:使尾气中NO、NO2被充分吸收;Ca(OH)2;
(3)若n(NO):n(NO2)>1:1,则一氧化氮过量,排放气体中NO含量升高;若n(NO):n(NO2)<1:1,则二氧化氮过量,二氧化氮可与石灰乳反应生成Ca(NO3)2,故答案为:排放气体中NO含量升高;产品Ca(NO2)2中Ca(NO3)2含量升高;
(4)反应物是NO2-和H+,生成物是一氧化氮,硝酸根和水,反应的离子方程式为3NO2-+2H+=NO3-+2NO↑+H2O,故答案为:3NO2-+2H+=NO3-+2NO↑+H2O.
| c(N2O3) |
| c(NO)?c(NO2) |
| c(N2O3) |
| c(NO)?c(NO2) |
(2)使尾气中NO、NO2与石灰乳充分接触,NO、NO2被充分吸收;滤渣主要成分是Ca(OH)2,故答案为:使尾气中NO、NO2被充分吸收;Ca(OH)2;
(3)若n(NO):n(NO2)>1:1,则一氧化氮过量,排放气体中NO含量升高;若n(NO):n(NO2)<1:1,则二氧化氮过量,二氧化氮可与石灰乳反应生成Ca(NO3)2,故答案为:排放气体中NO含量升高;产品Ca(NO2)2中Ca(NO3)2含量升高;
(4)反应物是NO2-和H+,生成物是一氧化氮,硝酸根和水,反应的离子方程式为3NO2-+2H+=NO3-+2NO↑+H2O,故答案为:3NO2-+2H+=NO3-+2NO↑+H2O.
点评:本题考查学生在“工艺流程阅读分析,化学反应原理在工艺流程的应用,氧化还原反应分析,相关反应的书写”等方面对元素化合物性质及其转化关系的理解和应用程度,考查学生对新信息的处理能力,题目难度适中.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
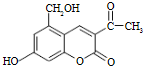 (2012?江苏一模)亮菌甲素为利胆解痉药适用于急性胆囊炎治疗等,其结构简式如图.下列有关叙述正确的是( )
(2012?江苏一模)亮菌甲素为利胆解痉药适用于急性胆囊炎治疗等,其结构简式如图.下列有关叙述正确的是( )