题目内容
X、Y、Z为三种常见短周期元素,它们位于同一周期,且原子序数依次增大,X的最高价氧化物对应的水化物为强碱,Y、Z的最高价氧化物对应的水化物均为强酸,W与Z同主族,且其原子序数相差18.请回答下列问题:
(1)Z的含氧酸中相对分子质量最小的是
(2)X2Y与W2在水溶液中反应的离子方程式为
(3)如图装置(Ⅰ)是一种可充电电池的示意图,装置(Ⅱ)为电解池的示意图.装置(Ⅰ)的离子交换膜只允许X+通过.电池充电、放电的电池反应为:X2Y4+3XW
2X2Y2+XW3,当闭合K时,X及附近溶液变红色.下列说法正确的是

A.闭合K时,X+从右到左通过离子交换膜
B.闭合K时,负极反应为3XW-2e-=XW3+2X+
C.闭合K时,X电极的电极反应为2Cl-2e-=Cl2↑
D.闭合K时,当有0.1mol X+通过离子交换膜,X电极上析出标准状况下气体1.12L.
(1)Z的含氧酸中相对分子质量最小的是
HClO
HClO
.(填化学式)(2)X2Y与W2在水溶液中反应的离子方程式为
S2-+Br2═S↓+2Br-
S2-+Br2═S↓+2Br-
.(3)如图装置(Ⅰ)是一种可充电电池的示意图,装置(Ⅱ)为电解池的示意图.装置(Ⅰ)的离子交换膜只允许X+通过.电池充电、放电的电池反应为:X2Y4+3XW
| 充电 | 放电 |
D
D
.
A.闭合K时,X+从右到左通过离子交换膜
B.闭合K时,负极反应为3XW-2e-=XW3+2X+
C.闭合K时,X电极的电极反应为2Cl-2e-=Cl2↑
D.闭合K时,当有0.1mol X+通过离子交换膜,X电极上析出标准状况下气体1.12L.
分析:X、Y、Z为三种常见短周期元素,它们位于同一周期,且原子序数依次增大,X的最高价氧化物对应的水化物为强碱,Y、Z的最高价氧化物对应的水化物均为强酸,W与Z同主族,且其原子序数相差18,则Z属于第三周期元素,X对应的碱是强碱,则X是钠元素,Y的原子序数小于Z,则Y、Z的最高价氧化物对应的水化物均为强酸,所以Y是硫元素,Z是氯元素,W是溴元素.
解答:解:X、Y、Z为三种常见短周期元素,它们位于同一周期,且原子序数依次增大,X的最高价氧化物对应的水化物为强碱,Y、Z的最高价氧化物对应的水化物均为强酸,W与Z同主族,且其原子序数相差18,则Z属于第三周期元素,X对应的碱是强碱,则X是钠元素,Y的原子序数小于Z,则Y、Z的最高价氧化物对应的水化物均为强酸,所以Y是硫元素,Z是氯元素,W是溴元素.
(1)Z的含氧酸中相对分子质量最小的应该是含有氧原子个数最少的,所以是HClO,故答案为:HClO;
(2)硫化钠具有还原性,溴具有氧化性,所以硫化钠能被溴氧化生成硫单质,同时自身被还原生成溴离子,反应离子反应方程式为:S2-+Br2═S↓+2Br-,故答案为:S2-+Br2═S↓+2Br-;
(3)I是原电池,II是电解池,当闭合K时,X及附近溶液变红色则X电极是阴极,阴极上氢离子放电,Y电极是阳极,A是负极,B是正极
A.闭合K时,X+向正极移动,所以应该是从左到右通过离子交换膜,故错误;
B.闭合K时,负极上失电子化合价升高而发生氧化反应,故错误;
C.闭合K时,X电极上氢离子放电生成氢气,故错误;
D.闭合K时,当有0.1mol X+通过离子交换膜,X电极上析出标准状况下气体=
×22.4L/mol=1.12L,故正确;
故选D.
(1)Z的含氧酸中相对分子质量最小的应该是含有氧原子个数最少的,所以是HClO,故答案为:HClO;
(2)硫化钠具有还原性,溴具有氧化性,所以硫化钠能被溴氧化生成硫单质,同时自身被还原生成溴离子,反应离子反应方程式为:S2-+Br2═S↓+2Br-,故答案为:S2-+Br2═S↓+2Br-;
(3)I是原电池,II是电解池,当闭合K时,X及附近溶液变红色则X电极是阴极,阴极上氢离子放电,Y电极是阳极,A是负极,B是正极
A.闭合K时,X+向正极移动,所以应该是从左到右通过离子交换膜,故错误;
B.闭合K时,负极上失电子化合价升高而发生氧化反应,故错误;
C.闭合K时,X电极上氢离子放电生成氢气,故错误;
D.闭合K时,当有0.1mol X+通过离子交换膜,X电极上析出标准状况下气体=
| 0.1mol |
| 2 |
故选D.
点评:本题考查了元素的推断及原电池和电解池原理,根据元素周期律及原电池和电解池原理来分析解答即可,注意原电池放电时,电解质溶液中阴阳离子的移动方向,为易错点.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
( 7分)X、Y、Z为三种常见短周期元素,它们位于同一周期,且原子序数依次增大,X的最高价氧化物对应的水化物为强碱,Y、Z的最高价氧化物对应的水化物均为强酸,W与Z同主族,且其原子序数相差18。请回答下列问题:
(1)Z的含氧酸中相对分子质量最小的是_____________________。(填化学式)
(2)X2Y与W2在水溶液中反应的离子方程式为_________________________________。
(3)下图装置(Ⅰ)是一种可充电电池的示意图,装置(Ⅱ)为电解池的示意图。装置(Ⅰ)的离子交换膜只允许X+通过。电池充电、放电的电池反应为:
当闭合K时,X及附近溶液变红色。下列说法正确的是____________________。
| A.闭合K时,X+从右到左通过离子交换膜 |
| B.闭合K时,负极反应为3XW-2e-=XW3+2X+ |
| C.闭合K时,X电极的电极反应为2Cl-2e-=Cl2↑ |
D.闭合K时,当有0.1mol X+通过离子交换膜,X电极 上析出标准状况下气体1 上析出标准状况下气体1 .12L .12L |
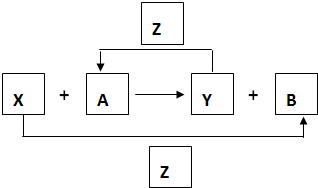 X、Y、Z为三种常见的单质,Z为绿色植物光合作用后的产物之一,A、B为常见的化合物.它们在一定条件下可以发生如图所示的转化关系(均不是在溶液中进行的反应,以下每空中填入一种即可).
X、Y、Z为三种常见的单质,Z为绿色植物光合作用后的产物之一,A、B为常见的化合物.它们在一定条件下可以发生如图所示的转化关系(均不是在溶液中进行的反应,以下每空中填入一种即可). 的单质,Z为绿色植物光合作用后的产物之一,A、B为常见的化合物。它们在一定条件下可以发生如图所示的转化关系(均不是在溶液中进行的反应)以下每空中填入一种即可)。
的单质,Z为绿色植物光合作用后的产物之一,A、B为常见的化合物。它们在一定条件下可以发生如图所示的转化关系(均不是在溶液中进行的反应)以下每空中填入一种即可)。
 为
为 固体时,X与A反应的化学方程式为
固体时,X与A反应的化学方程式为