题目内容
某固体可能由Na2SO4、NaCl、Na2CO3、KNO3中的一种或几种组成,现进行如下实验:
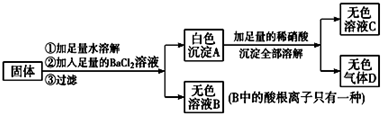
试完成下列问题:
(1)白色沉淀A的化学式为
(2)原固体中一定含有
(3)为检验上述可能含有的物质是否一定存在,某同学又设计了如下实验方案:
①取少量固体溶于水,加入足量的Ba(NO3)2溶液,充分反应后,过滤;
②取滤液加入AgNO3溶液,观察有无白色沉淀生成,由此得出结论.
在上述某同学的实验方案①中,加入足量的Ba(NO3)2溶液的目的是

试完成下列问题:
(1)白色沉淀A的化学式为
BaCO3
BaCO3
,无色气体D的化学式为CO2
CO2
.(2)原固体中一定含有
Na2CO3
Na2CO3
,一定不含有Na2SO4、KNO3
Na2SO4、KNO3
,可能含有NaCl
NaCl
.(3)为检验上述可能含有的物质是否一定存在,某同学又设计了如下实验方案:
①取少量固体溶于水,加入足量的Ba(NO3)2溶液,充分反应后,过滤;
②取滤液加入AgNO3溶液,观察有无白色沉淀生成,由此得出结论.
在上述某同学的实验方案①中,加入足量的Ba(NO3)2溶液的目的是
反应除去原溶液中Na2CO3,排除干扰
反应除去原溶液中Na2CO3,排除干扰
.分析:根据白色沉淀溶于稀硝酸的性质即可判定它是碳酸钡,则原固体中一定不含Na2SO4,肯定含有Na2CO3;根据无色溶液B中只含有一种酸根离子,由Na2CO3和BaCl2溶液反应得到无色溶液B,可知这种酸根离子只能是Cl-,则固体中一定不含KNO3,可能含有NaCl,然后根据问题回答.
解答:解:(1)因固体中有Na2SO4、Na2CO3,若向固体配得的溶液中滴加BaCl2溶液,则会产生白色沉淀BaSO4、BaCO3,滴加稀HNO3后沉淀全部溶解,说明白色沉淀为BaCO3,则原固体中一定不含Na2SO4,肯定含有Na2CO3.
故答案为:BaCO3;CO2;
(2)又因无色溶液B中只含有一种酸根离子,由Na2CO3和BaCl2溶液反应得到无色溶液B,可知这种酸根离子只能是Cl-,逆推固体中一定不含KNO3,可能含有NaCl.
故答案为:Na2CO3;Na2SO4、KNO3;NaCl;
(3)为了检验NaCl是否存在,可向溶液中加入足量Ba(NO3)2或稀HNO3除去Na2CO3后,再滴加AgNO3溶液检验.
故答案为:反应除去原固体中Na2CO3,排除干扰.
故答案为:BaCO3;CO2;
(2)又因无色溶液B中只含有一种酸根离子,由Na2CO3和BaCl2溶液反应得到无色溶液B,可知这种酸根离子只能是Cl-,逆推固体中一定不含KNO3,可能含有NaCl.
故答案为:Na2CO3;Na2SO4、KNO3;NaCl;
(3)为了检验NaCl是否存在,可向溶液中加入足量Ba(NO3)2或稀HNO3除去Na2CO3后,再滴加AgNO3溶液检验.
故答案为:反应除去原固体中Na2CO3,排除干扰.
点评:本题主要是考查同学们的综合分析能力,不但要求同学们具备有关化合物的基础知识,而且要有实验操作的经历和分析、解决化学实验问题的能力,解题时需要认真分析题目给出的条件,联系实际,逐一分析推断.

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目