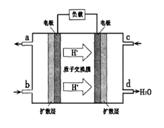
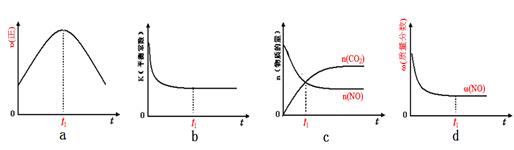
题目内容
下列说法或表示方法正确的是
| A.反应物的总能量低于生成物的总能量时,该反应一定不能发生 |
| B.在10l kPa、25 ℃时,1 g H2完全燃烧生成气态水,放出120.9 kJ的热量,则氢气的燃烧热为241.8 kJ/mol |
C.已知:2SO2 (g) + O2 (g)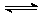 2SO3 (g) ;△H =-98.3 kJ/mol。将1 mol SO2和0.5 mol O2充入一密闭容器中反应,放出49.15 kJ 的热量 2SO3 (g) ;△H =-98.3 kJ/mol。将1 mol SO2和0.5 mol O2充入一密闭容器中反应,放出49.15 kJ 的热量 |
| D.由石墨比金刚石稳定可知:C(金刚石,s)= C(石墨,s) ;△H<0 |
D
试题分析:A、反应物的总能量低于生成物的总能量为吸热反应,有可能发生,错误;B、燃烧热为1mol燃料完全燃烧,生成稳定的产物时得反应热,所以生成气态水的反应热不是燃烧热,错误;C、因为SO2与O2的反应为可逆反应,1 mol SO2和0.5 mol O2不可能完全反应,放出的热量要小于49.15kJ;D、石墨比金刚石稳定,说明石墨的能量低于金刚石,所以金刚石转化为石墨为放热反应,△H<0,正确。

练习册系列答案
相关题目
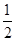 H2SO4(aq)+
H2SO4(aq)+ 2NO △H=+180 kJ/mol,其中N≡N,O=O键的键能分别是946 kJ/mol、498 kJ/mol,则NO中化学键的键能为
2NO △H=+180 kJ/mol,其中N≡N,O=O键的键能分别是946 kJ/mol、498 kJ/mol,则NO中化学键的键能为