题目内容
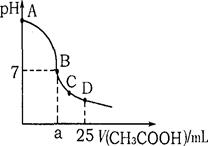
用0.01 mol/L H2SO4滴定0.01mol/L NaOH溶液,中和后加水至100ml,若滴定时终点判断有误差:①多加1滴H2SO4;②少加1滴H2SO4;(设1滴为0.05ml)则①和②c(H+)的比值是
| A.10 | B.50 | C.5×103 | D.104 |
D
多加1滴硫酸,则溶液中氢离子的浓度为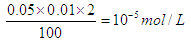 。同样少加1滴硫酸,溶液中OH-的浓度就应该是10-5mol/L,则①和②c(H+)的比值是104。答案选D。
。同样少加1滴硫酸,溶液中OH-的浓度就应该是10-5mol/L,则①和②c(H+)的比值是104。答案选D。
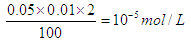 。同样少加1滴硫酸,溶液中OH-的浓度就应该是10-5mol/L,则①和②c(H+)的比值是104。答案选D。
。同样少加1滴硫酸,溶液中OH-的浓度就应该是10-5mol/L,则①和②c(H+)的比值是104。答案选D。
练习册系列答案
相关题目
 的稀溶液中
的稀溶液中 已知
已知 向该溶液中逐滴加入PH=c的盐液,测得混合溶液的部分PH如下表所示
向该溶液中逐滴加入PH=c的盐液,测得混合溶液的部分PH如下表所示 溶液体积/ml
溶液体积/ml