题目内容
在一定条件下,将70ml硫化氢气体和90ml氧气混合,点燃并使其反应,再恢复到原来的条件,则生成的SO2气体的体积为( )A.70mL
B.60mL
C.50mL
D.55mL
【答案】分析:根据O2过量有:2H2S+3O2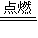 2SO2+2H2O,O2不足有:2H2S+O2
2SO2+2H2O,O2不足有:2H2S+O2 2S↓+2H2O判断该反应介于两者之间,所以可以设反应方程式为:7H2S+9O2=xS↓+ySO2+zH2O通过方程式组来求解.
2S↓+2H2O判断该反应介于两者之间,所以可以设反应方程式为:7H2S+9O2=xS↓+ySO2+zH2O通过方程式组来求解.
解答:解:设反应方程式为:7H2S+9O2=xS↓+ySO2+zH2O,那么有
x+y=7
z=7
2y+z=18
所以x=1.5,y=5.5,z=7
所以SO2气体体积就是5.5*10=55ml,故选:D;
点评:本题主要考查了反应的过量判断以及质量守恒的运用,难度中等.
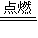 2SO2+2H2O,O2不足有:2H2S+O2
2SO2+2H2O,O2不足有:2H2S+O2 2S↓+2H2O判断该反应介于两者之间,所以可以设反应方程式为:7H2S+9O2=xS↓+ySO2+zH2O通过方程式组来求解.
2S↓+2H2O判断该反应介于两者之间,所以可以设反应方程式为:7H2S+9O2=xS↓+ySO2+zH2O通过方程式组来求解.解答:解:设反应方程式为:7H2S+9O2=xS↓+ySO2+zH2O,那么有
x+y=7
z=7
2y+z=18
所以x=1.5,y=5.5,z=7
所以SO2气体体积就是5.5*10=55ml,故选:D;
点评:本题主要考查了反应的过量判断以及质量守恒的运用,难度中等.

练习册系列答案
相关题目