题目内容
有氯化铝、偏铝酸钠、氯化钡、碳酸钠四种无色溶液。只需用下列1种试剂即可一次鉴别,这种试剂是
| A.稀硫酸 | B.硝酸银溶液 | C.氢氧化钠溶液 | D.稀硝酸 |
A
解析试题分析:进行物质的检验时,要依据物质的特殊性质和特征反应,选择适当的试剂和方法,准确观察反应中的明显现象,如颜色的变化、沉淀的生成和溶解、气体的产生和气味、火焰的颜色等,进行判断、推理、验证即可。A、稀硫酸与氯化铝不反应,与偏铝酸钠反应生成白色沉淀氢氧化铝,稀硫酸过量时沉淀又溶解。与氯化钡反应生成白色沉淀硫酸钡。与碳酸钠反应生成CO2气体,实验现象各不相同,可以鉴别,A正确;B、硝酸银与偏铝酸钠不反应,与另外三种物质均反应生成白色沉淀,不能鉴别,B不正确;C、氢氧化钠溶液与氯化铝反应生成白色沉淀,氢氧化钠过量时沉淀溶解。与偏铝酸钠、氯化钡、碳酸钠均不反应,不能鉴别,C不正确;D、稀硝酸与氯化铝不反应,与偏铝酸钠反应生成白色沉淀氢氧化铝,稀硝酸过量时沉淀又溶解。与氯化钡不反应。与碳酸钠反应生成CO2气体,不能鉴别,D不正确,答案选A。
考点:考查物质鉴别的正误判断

练习册系列答案
相关题目
海水淡化的研究已经有很长时间的历史了,通过海水淡化可以部分解决淡水紧缺的问题。下列可以实现海水淡化的实验操作是
| A.过滤 | B.蒸发 | C.蒸馏 | D.萃取 |
下列除去杂质的方法中,正确的是
| 选项 | 物质(括号内为杂质) | 试剂 | 方法 |
| A | Cl2(HCl ) | NaOH溶液 | 洗气 |
| B | Fe(Al) | NaOH溶液 | 过滤 |
| C | CO2(CO) | O2 | 点燃 |
| D | KNO3(KOH) | FeCl3溶液 | 过滤 |
除去下列物质中少量杂质的方法正确的是
| A.除去CO2中混有的HCl:用饱和碳酸钠溶液洗气 |
| B.除去KCl溶液中混有的K2SO4:加入过量BaCl2溶液,过滤 |
| C.除去FeCl2溶液中混有的FeCl3:加入过量铁粉,过滤 |
| D.除去NaHCO3中混有的Na2CO3:用加热法 |
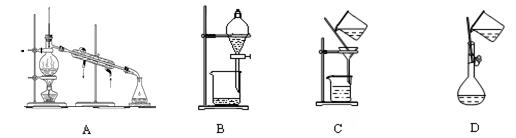
用下列分离装置进行相应实验,能达到相应实验目的的是
| A.用图Ⅰ所示装置除去CO2中含有的少量HCl |
| B.用图Ⅱ所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
| C.用图Ⅲ所示装置分离NaCl和Na2SO4的混合溶液 |
| D.用图Ⅳ所示装置分离CCl4萃取碘水中的碘后已分层的有机层和水层 |
除去下列各组物质中的杂质选用的试剂和方法均最合理的是
| | 物质 | 杂质 | 试剂 | 方法 |
| A | 苯 | 苯酚 | 溴水 | 过滤 |
| B | 二氧化碳 | 二氧化硫 | 澄清石灰水 | 洗气 |
| C | 氧化铁 | 二氧化硅 | 氢氧化钠溶液 | 过滤 |
| D | 乙酸乙酯 | 乙酸 | 饱和碳酸钠溶液 | 蒸馏 |
为了证明硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O]晶体的成分中含有NH4+、Fe2+、SO42-和H2O,下列实验叙述中不正确的是
| A.取少量硫酸亚铁铵晶体放入试管中,加热,试管口有液体生成,则可证明晶体的成分中含有结晶水 |
| B.取少量硫酸亚铁铵晶体放入试管,加浓NaOH溶液,加热,试管口湿润的蓝色石蕊试纸变红,则可证明晶体的成分中含有NH4+ |
| C.取适量硫酸亚铁铵晶体溶于水,加少量稀盐酸,无现象,再滴入几滴BaCl2溶液,有白色沉淀生成,则可证明晶体的成分中含有SO42- |
| D.取适量硫酸亚铁铵晶体溶于水,得浅绿色溶液,滴入2滴KSCN溶液,溶液不显血红色,再滴入几滴新制氯水,溶液变为血红色,则可证明晶体的成分中含有Fe2+ |
下列装置或操作错误的是(双选) ( )。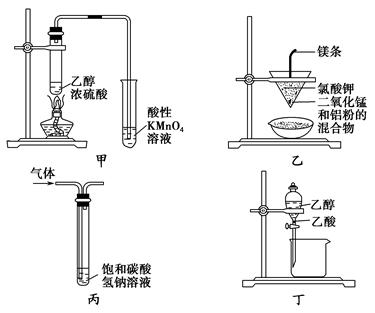
| A.甲图所示装置可以检验有乙烯生成 |
| B.乙图所示装置可以制取金属锰 |
| C.丙图所示装置用来洗气,除去CO2中的HCl气体 |
| D.丁图所示装置用来分离乙醇和乙酸 |