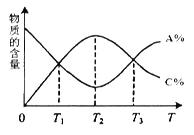��Ŀ����
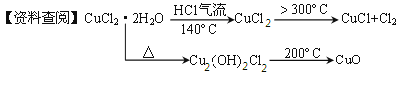
����Ŀ��CuCl�㷺Ӧ���ڻ�����ӡȾ����ҵ��ij�о���ѧϰС�����ȷֽ�CuCl2��2H2O�Ʊ�CuCl�����������̽����
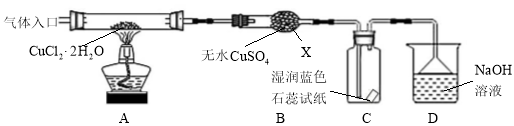
��ʵ��̽������С������ͼ��ʾװ�ý���ʵ��(�г�������)��
��ش��������⣺
(1)����X��������__________��
(2)ʵ��������Ⱥ�˳���Ǣ� �� �� �� �� �ݡ�
�ټ��װ�õ������Ժ����ҩƷ ��Ϩ��ƾ��ƣ���ȴ
���ڡ�������ڡ���ͨ����HCl �ܵ�ȼ�ƾ��ƣ�����
��ֹͣͨ��HCl��Ȼ��ͨ��N2
(3)��ʵ������У��۲쵽B�������ɰ�ɫ��Ϊ��ɫ��C����ֽ����ɫ�仯�� ��
(4)װ��D�з�����Ӧ�����ӷ���ʽ�� ��
(5)��Ӧ������ȡ��CuCl��Ʒ����ʵ�飬�������к���������CuCl2��CuO���ʣ�����������Ϣ������
����������CuCl2���������ԭ���� ��
����������CuO���������ԭ���� ��
(6)����֤ʵ����ΪCuO����д����Cu2(OH)2Cl 2����CuO�Ļ�ѧ����ʽ ��
���𰸡�
(1)�����������(2)������������(3)�ȱ�����ɫ��
(4)Cl2+2OH-=Cl-+ClO-+2H2O��H++OH-=H2O��
(5)������ʱ�䲻����¶�ƫ������HCl�������㡣
(6)Cu2(OH)2Cl2![]() 2CuO+2HCl����
2CuO+2HCl����
��������
���������(1)��ͼ��������������֪������X������Ϊ���θ���ܣ��ʴ�Ϊ�����θ���ܣ�
(2)ʵ�������������ɣ��ȼ���װ�õ������ԣ����ȷֽ�CuCl22H2O�Ʊ�CuCl����ֹCuCl��������Cu+ˮ�����Ա���Ҫ�ȸ���װ���е�������ˮ������ż��ȣ���Ҫ��HCl�����м����Ʊ�����Ӧ��������Ϩ��ƾ��ƣ�Ӧ��Ҫ����ͨ�뵪��ֱ��װ�����У����Բ���˳��Ϊ���� �������������� �����ʴ�Ϊ��������������
(3)B���а�ɫ��Ϊ��ɫ��˵����ˮ���ɣ������л���Cl2������C��ʯ����ֽ����Ϊ��ɫ������ɫ���ʴ�Ϊ��ʯ����ֽ����Ϊ��ɫ������ɫ��
(4)D����Cl2��NaOH��Ӧ�����Ȼ��ơ��������ƺ�ˮ�����Ȼ������������Ƶķ�Ӧ����Ӧ�����ӷ���ʽΪCl2+2OH-=Cl-+ClO-+H2O��H++OH-=H2O���ʴ�Ϊ��Cl2+2OH-=Cl-+ClO-+H2O��H++OH-=H2O��
(5)����2CuCl2![]() 2CuCl+Cl2����������CuCl2˵��CuCl2û�з�Ӧ��ȫ���ֽ��¶Ȳ��ߣ��ʴ�Ϊ������ʱ�䲻����¶�ƫ�ͣ�������������ͭ��˵��CuCl�����������Ų�����CuO��˵��װ������������������û����HCl�ķ�Χ�м��Ȼ���δ���Թ���ȴ��ֹͣͨ��HCl���壬�ʴ�Ϊ��ͨ��HCl�������㡣
2CuCl+Cl2����������CuCl2˵��CuCl2û�з�Ӧ��ȫ���ֽ��¶Ȳ��ߣ��ʴ�Ϊ������ʱ�䲻����¶�ƫ�ͣ�������������ͭ��˵��CuCl�����������Ų�����CuO��˵��װ������������������û����HCl�ķ�Χ�м��Ȼ���δ���Թ���ȴ��ֹͣͨ��HCl���壬�ʴ�Ϊ��ͨ��HCl�������㡣
(6)����֤ʵ����ΪCuO������Cu2(OH)2Cl 2����CuO�Ļ�ѧ����ʽΪCu2(OH)2Cl2![]() 2CuO+2HCl�����ʴ�Ϊ��Cu2(OH)2Cl2
2CuO+2HCl�����ʴ�Ϊ��Cu2(OH)2Cl2![]() 2CuO+2HCl����
2CuO+2HCl����