题目内容
最近有人用一种称为“超酸”化合物[H(CB11H6Cl6)]和C60反应,使C60获得一个质子,得到一种新型离子化合物[HC60]+[CB11H6Cl6]-.这个反应跟下列哪一个化学反应最相似( )A.HCl+NH3=NH4Cl
B.SO3+H2O=H2SO4
C.CH2=CH2+HCl→CH3CH2Cl
D.2Na+Cl2
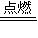 2NaCl
2NaCl
【答案】分析:根据化学反应的本质反应前为两种共价化合物,通过得失质子得到一种离子化合物,从选项中根据特征选出正确答案
解答:解:A.氨气分子得到一个质子生成铵根离子,氯化氢分子失去一个质子后只剩余氯离子,形成离子化合物如题干中的新型化合物,故A选;
B.三氧化硫与水反应生成了共价化合物硫酸,故B不选;
C.乙烯与氯化氢反应生成氯乙烷,氯乙烷为共价化合物,与题意离子化合物不符,故C不选;
D.钠失去电子,氯气得电子,生成氯化钠,其中得失的为电子,不是质子,故D不选;
故选A.
点评:本题考查了化学反应的本质,根据已知化学反应的特征判断选项中具有相同特征的化学反应.
解答:解:A.氨气分子得到一个质子生成铵根离子,氯化氢分子失去一个质子后只剩余氯离子,形成离子化合物如题干中的新型化合物,故A选;
B.三氧化硫与水反应生成了共价化合物硫酸,故B不选;
C.乙烯与氯化氢反应生成氯乙烷,氯乙烷为共价化合物,与题意离子化合物不符,故C不选;
D.钠失去电子,氯气得电子,生成氯化钠,其中得失的为电子,不是质子,故D不选;
故选A.
点评:本题考查了化学反应的本质,根据已知化学反应的特征判断选项中具有相同特征的化学反应.

练习册系列答案
相关题目
 H3O++CH3COO-
H3O++CH3COO-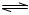 H3O+
+CH3COO -
H3O+
+CH3COO -