题目内容
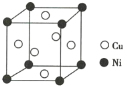
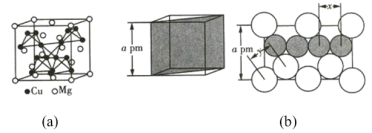
【题目】(1)图(a)是MgCu2的拉维斯结构,Mg以金刚石方式堆积,八面体空隙和半数的四面体空隙中,填入以四面体方式排列的Cu。图(b)是沿立方格子对角面取得的截图。可见,Cu原子之间最短距离x=_________pm,Mg原子之间最短距离y=_________pm。设阿伏加德罗常数的值为NA,则MgCu2的密度是_________g·cm-3(列出计算表达式)。
(2)一种四方结构的超导化合物的晶胞如图1所示。晶胞中Sm和As原子的投影位置如图2所示。图中F-和O2-共同占据晶胞的上下底面位置,若两者的比例依次用x和1-x代表,则该化合物的化学式表示为__________;通过测定密度![]() 和晶胞参数,可以计算该物质的x值,完成它们关系表达式:ρ=____g·cm-3。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图1中原子的坐标为(
和晶胞参数,可以计算该物质的x值,完成它们关系表达式:ρ=____g·cm-3。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图1中原子的坐标为(![]() ,
,![]() ,
,![]() )则原子2和3的坐标分别为__________、__________。
)则原子2和3的坐标分别为__________、__________。

【答案】![]()
![]()
![]() SmFeAsO1-xFx
SmFeAsO1-xFx 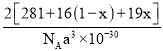 (
(![]() ,
,![]() ,0) (0,0,
,0) (0,0,![]() )
)
【解析】
(1)如图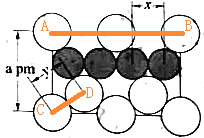 所示,AB之间的距离为面对角线长度=
所示,AB之间的距离为面对角线长度=![]() a pm,AB之间距离相当于4个Cu原子直径,x距离1个Cu原子直径=
a pm,AB之间距离相当于4个Cu原子直径,x距离1个Cu原子直径=![]() pm,体对角线长度=
pm,体对角线长度=![]() 棱长=
棱长=![]() a pm;CD距离为y,该长度为体对角线BC长度的
a pm;CD距离为y,该长度为体对角线BC长度的![]() =
=![]() ×
×![]() a pm=
a pm=![]() pm,该晶胞中Mg原子位于8个顶点上、6个面心上,在晶胞内部有4个Mg原子,所以Mg原子个数=8×
pm,该晶胞中Mg原子位于8个顶点上、6个面心上,在晶胞内部有4个Mg原子,所以Mg原子个数=8×![]() +6×
+6×![]() +4=8,Cu原子都位于晶胞内部,有16个;晶胞体积V=(a×10-10 cm)3,晶胞密度ρ=
+4=8,Cu原子都位于晶胞内部,有16个;晶胞体积V=(a×10-10 cm)3,晶胞密度ρ=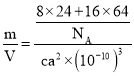 g/cm3=
g/cm3=![]() g/cm3;
g/cm3;
(2)由晶胞结构中各原子所在位置可知,该晶胞中Sm个数为![]() ,Fe个数为
,Fe个数为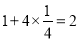 ,As个数为
,As个数为![]() ,O和F的个数之和为2,F-的比例为x,O2-的比例为1-x,故该化合物的化学式为 SmFeAsO1-xFx ,1个晶胞的质量为
,O和F的个数之和为2,F-的比例为x,O2-的比例为1-x,故该化合物的化学式为 SmFeAsO1-xFx ,1个晶胞的质量为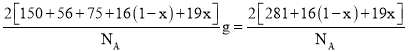 g,1个晶胞的体积为V=(a×10-10 pm)3= a3×10-30 cm3,则晶胞密度ρ=
g,1个晶胞的体积为V=(a×10-10 pm)3= a3×10-30 cm3,则晶胞密度ρ=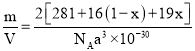 g/cm3;原子2位于底面面心,其坐标为(
g/cm3;原子2位于底面面心,其坐标为(![]() ,
,![]() ,0);原子3位于棱上,其坐标为(0,0,
,0);原子3位于棱上,其坐标为(0,0,![]() )。
)。

 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案