题目内容
【题目】2010年,中国首次应用六炔基苯在铜片表面合成了石墨炔薄膜(其合成示意图如图所示),其特殊的电子结构将有望广泛应用于电子材料领域.下列说法不正确的是( ) 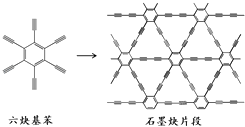
A.六炔基苯的化学式为C18H6
B.六炔基苯和石墨炔都具有平面型结构
C.六炔基苯和石墨炔都可发生加成反应
D.六炔基苯合成石墨炔属于加聚反应
【答案】D
【解析】解:A.六炔基苯含有18个C原子、6个H原子,分子式为C18H6 , 故A正确;
B.苯为平面结构,乙炔为直线型结构,六炔基苯和石墨炔都具有平面型结构,故B正确;
C.六炔基苯和石墨炔均含有苯环、碳碳三键,都可发生加成反应,故C正确;
D.由结构可知,六炔基苯合成石墨炔有氢气生成,不属于加聚反应,故D错误,
故选:D.
A.六炔基苯含有18个C原子、6个H原子;
B.苯为平面结构,乙炔为直线型结构;
C.六炔基苯和石墨炔均含有苯环、碳碳三键;
D.由结构可知,六炔基苯合成石墨炔有氢气生成.

 同步奥数系列答案
同步奥数系列答案【题目】工业上一般在恒容密闭容器中采用下列反应合成甲醇:CO(g)+2H2(g)CH3OH(g)
(1)判断反应达到平衡状态的依据是(填字母序号,下同) .
A.生成CH3OH的速率与消耗CO的速率相等
B.混合气体的密度不变
C.混合气体的相对平均分子质量不变
D.CH3OH,CO,H2的浓度都不再发生变化
E.气体的压强不再改变
(2)表所列数据是该反应在不同温度下的化学平衡常数(K).
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.2mol/L,则CO的转化率为 , 此时的温度为 .
(3)要提高CO的转化率,可以采取的措施是 .
a.升温 b.加入催化剂 c.增加CO的浓度 d.恒容下加入H2使压强变大
e.恒容下加入惰性气体使压强变大 f.分离出甲醇
(4)在250℃时,测得某密闭容器中各物质的物质的量浓度见表:
CO | H2 | CH3OH |
0.5molL﹣1 | 2molL﹣1 | 6molL﹣1 |
此时反应的正、逆反应速率的关系是:v(正)v(逆)(填“>”“<”或“═”).