题目内容
在100℃时,将0.40 mol二氧化氮气体充入一个1 L抽空的密闭容器中,发生反应:2NO2 N2O4。每隔一段时间就对该容器内的物质进行分析,得到下表数据:
N2O4。每隔一段时间就对该容器内的物质进行分析,得到下表数据:
时间/s | 0 | 20 | 40 | 60 | 80 |
n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
(1)在上述条件下,从反应开始至20 s时,用NO2表示的平均反应速率为_____________。
(2)该反应的平衡常数K的数值为___________(精确到0.1)。
(3)若在相同条件下最初向该容器中充入N2O4,要达到上述平衡状态,N2O4的起始浓度是______mol·L?1。
(4)上述(3)达到平衡后N2O4的转化率为_______,混合气体的平均摩尔质量为____________。
(5)达到平衡后,如果升高温度,气体颜色会变深,则升高温度后,反应2NO2 N2O4的平衡常数将________(填“增大”“减小”或“不变”)。
N2O4的平衡常数将________(填“增大”“减小”或“不变”)。
(6)达到平衡后,如果向该密闭容器中再充入0.32 mol He,并把容器体积扩大为4 L,则平衡将_____(填“向左移动”“向右移动”或“不移动”)。
练习册系列答案
相关题目
仅用下表提供的玻璃仪器(非玻璃仪器任选),就能实现相应实验目的的是
选项 | 实验目的 | 玻璃仪器 |
A | 将溴水滴入KI溶液中,从溶液中分离生成的I2 | 胶头滴管、试管、漏斗、玻璃棒、烧杯 |
B | 实验室通过蒸馏的方法除去自来水中含有的Cl-等杂质制取蒸馏水 | 酒精灯、圆底烧瓶、冷凝管、尾接管、锥形瓶 |
C | 用植物油提取溴水中的Br2 | 铁架台、分液漏斗、玻璃棒、烧杯 |
D | 用浓氨水和氢氧化钠固体制取氨气 | 酒精灯、烧杯、导管、集气瓶 |
A. A B. B C. C D. D


 溶液中,CH3COOH分子数为NA
溶液中,CH3COOH分子数为NA

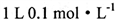 的NH4NO3溶液中氮原子数小于0.2NA
的NH4NO3溶液中氮原子数小于0.2NA 分反应时转移的电子数为1.2NA
分反应时转移的电子数为1.2NA NH3(g)+H2S(g)在某一温度下达到平衡,下列各种情况中,能使化学平衡正向移动的是( )
NH3(g)+H2S(g)在某一温度下达到平衡,下列各种情况中,能使化学平衡正向移动的是( )