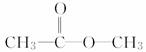
题目内容
以下是对化学反应变化过程及结果的研究。按要求回答问题:
Ⅰ.关于反应速率和限度的研究
(1)已知25℃时有关弱酸的电离平衡常数:
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
则等物质的量浓度的①CH3COONa、②NaCN、③Na2CO3、④NaHCO3溶液的pH由大到小的顺序为__________(填编号)。
(2)已知2SO2(g)+O2(g)2SO3(g) ΔH=-196.6 kJ·mol-1,在一个容积为2 L的容器中加入2 mol SO2和1 mol O2,在某温度下充分反应,经过30 min达到平衡,放出热量176.94 kJ。如果用SO2表示该反应的反应速率,则v(SO2)=________。
(3)下图为某温度下,CuS(s)、ZnS(s)、FeS(s)分别在溶液中达到沉淀溶解平衡后,溶液的S2-浓度、金属阳离子浓度变化情况。如果向三种沉淀中加盐酸,最先溶解的是________。
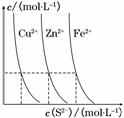
向新生成的ZnS浊液中滴入足量含相同浓度的Cu2+、Fe2+的溶液,振荡后,ZnS沉淀会转化为________(填化学式)沉淀。
Ⅱ.关于电化学的研究
全钒液流电池是一种新型的绿色环保储能电池。其电池总反应为:VO +2H++V2+
+2H++V2+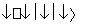 V3++VO2++H2O。则充电时阳极反应式为__________________________,用此电池电解1 L 1 mol·L-1的CuSO4溶液,当转移0.1 mol电子时,溶液的pH=________(不考虑溶液体积变化)。
V3++VO2++H2O。则充电时阳极反应式为__________________________,用此电池电解1 L 1 mol·L-1的CuSO4溶液,当转移0.1 mol电子时,溶液的pH=________(不考虑溶液体积变化)。
解析:Ⅰ.(1)酸越弱生成的钠盐碱性越强,所以pH由大到小的顺序为③②④①;
(2)放出热量176.94 kJ时二氧化硫参加反应的物质的量是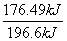 ×2 mol=1.8 mol,v(SO2)=
×2 mol=1.8 mol,v(SO2)=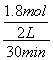 =0.03 mol·L-1·min-1;
=0.03 mol·L-1·min-1;
Ⅱ.充电时,阳极上失电子发生氧化反应,VO2++H2O-e-===VO +2H+;
+2H+;
硫酸铜溶液中硫酸铜的物质的量是1 mol,当转移0.1 mol电子时,溶液中阳极上析出0.025 mol氧气,同时生成0.1 mol氢离子,溶液中氢离子浓度=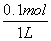 =0.1 mol·L-1,所以溶液的pH=1。
=0.1 mol·L-1,所以溶液的pH=1。
答案:Ⅰ.(1)③②④① (2)0.03 mol·L-1·min-1 (3)FeS CuS
Ⅱ.VO2++H2O-e-===VO +2H+ 1
+2H+ 1

在100℃时,将0.40 mol NO2气体充入2 L密闭容器中,每隔一段时间对该容器的物质进行测量,得到的数据如下表:
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)(mol) | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)(mol) | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
下列说法中正确的是( )
A.反应开始20 s内NO2的平均反应速率是0.0025 mol·L-1·s-1
B.80 s时混合气体的颜色与60 s时颜色相同,比40 s时的颜色深
C.80 s时向容器内加0.32 mol He,同时将容器扩大为4 L,则平衡不移动
D.若起始投料为0.20 mol N2O4,相同条件下达到平衡,则各组分的含量与原平衡相同
下列陈述I、Ⅱ正确并且有因果关系的是
| 选项 | 表述I | 表述II |
| A | SiO2有导电性 | SiO2可用于制备光导纤维 |
| B | SO2有漂白性 | SO2可使溴水褪色 |
| C | 溶液中含有大量的NO3- | 溶液中不能存在大量I-或S2- |
| D | 将淀粉与KCl混合液装于半透膜内,浸泡在盛 蒸馏水的烧杯中,5min后取烧杯中液体,加碘水变蓝色 | 半透膜有破损 |

 D.
D.