题目内容
1.下列化合物中既可以使KMnO4酸性溶液褪色,也可发生加成反应的是( )| A. | 乙烷 | B. | 乙醇 | C. | 丙烯 | D. | 苯 |
分析 既易发生加成反应,也能使KMnO4酸性溶液褪色,应为烯烃或炔烃类有机物,以此来解答.
解答 解:A.乙烷中不含不饱和键,不能发生加成反应,不能使KMnO4酸性溶液褪色,故A不选;
B.乙醇中不含不饱和键,不能发生加成反应,但-OH能使KMnO4酸性溶液褪色,故B不选;
C.丙烯中含碳碳双键,既易发生加成反应,也能使KMnO4酸性溶液褪色,故C选;
D.苯中不含双键,但能发生加成反应,不能使KMnO4酸性溶液褪色,故D不选;
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重不饱和烃性质的考查,题目难度不大.

练习册系列答案
相关题目
19.下列有关有机物的说法正确的是( )
| A. | 氯乙烯、聚乙烯均可使酸性高锰钾溶液褪色 | |
| B. | C2H6O2与C3H6O2一定属于同系物 | |
| C. | 苯可以与溴水、高锰酸钾溶液反应而使它们褪色 | |
| D. | CH3CH218OH和CH3COOH反应生成的水的相对分子质量为18 |
9. 水是生命的源泉、工业的血液、城市的血脉.要保护好河流,因为河水是主要的饮用水源,污染物通过饮用水可直接毒害人体,也可通过食物链和灌溉农田间接危及健康.请回答下列问题:
水是生命的源泉、工业的血液、城市的血脉.要保护好河流,因为河水是主要的饮用水源,污染物通过饮用水可直接毒害人体,也可通过食物链和灌溉农田间接危及健康.请回答下列问题:
(1)纯水在T℃时,pH=6,该温度下1mol•L-1的NaOH溶液中,由水电离出的c(OH-)=10-12 mol•L-1.
(2)25℃时,向水中加入少量碳酸钠固体,得到pH为11的溶液,其主要水解反应的离子方程式为CO32-+H2O?HCO3-+OH-、HCO3-+H2O?H2CO3+OH-,由水电离出的c(OH-)=0.001mol•L-1.
(3)体积均为100mL、pH均为2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数小于(填“大于”“小于”或“等于”)CH3COOH的电离平衡常数.理由是稀释相同倍数,一元酸HX的pH变化量比CH3COOH的小,故酸性较弱,电离平衡常数较小.
(4)电离平衡常数是衡量弱电解质电离程度的物理量.已知:
①25℃时,有等浓度的NaCN溶液、Na2CO3溶液和CH3COONa溶液,三溶液的pH由大到小的顺序为Na2CO3溶液>NaCN溶液>CH3COONa溶液(用化学式表示).
②向NaCN溶液中通入少量的CO2,发生反应的化学方程式为NaCN+H2O+CO2=HCN+NaHCO3.
(5)25℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)=9.9×10-7 mol•L-1(填精确值),c(CH3COO-)/c(CH3COOH)=18.
 水是生命的源泉、工业的血液、城市的血脉.要保护好河流,因为河水是主要的饮用水源,污染物通过饮用水可直接毒害人体,也可通过食物链和灌溉农田间接危及健康.请回答下列问题:
水是生命的源泉、工业的血液、城市的血脉.要保护好河流,因为河水是主要的饮用水源,污染物通过饮用水可直接毒害人体,也可通过食物链和灌溉农田间接危及健康.请回答下列问题:(1)纯水在T℃时,pH=6,该温度下1mol•L-1的NaOH溶液中,由水电离出的c(OH-)=10-12 mol•L-1.
(2)25℃时,向水中加入少量碳酸钠固体,得到pH为11的溶液,其主要水解反应的离子方程式为CO32-+H2O?HCO3-+OH-、HCO3-+H2O?H2CO3+OH-,由水电离出的c(OH-)=0.001mol•L-1.
(3)体积均为100mL、pH均为2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数小于(填“大于”“小于”或“等于”)CH3COOH的电离平衡常数.理由是稀释相同倍数,一元酸HX的pH变化量比CH3COOH的小,故酸性较弱,电离平衡常数较小.
(4)电离平衡常数是衡量弱电解质电离程度的物理量.已知:
| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
②向NaCN溶液中通入少量的CO2,发生反应的化学方程式为NaCN+H2O+CO2=HCN+NaHCO3.
(5)25℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)=9.9×10-7 mol•L-1(填精确值),c(CH3COO-)/c(CH3COOH)=18.
16.下列溶液中有关物质的浓度关系正确的是( )
| A. | c(NH4+)相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液中:c(NH4HSO4)>c>c(NH4Cl) | |
| B. | 向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | |
| C. | 等物质的量的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-) | |
| D. | 某二元弱酸的酸式盐NaHA溶液中:c(H+)+c(Na+)=c(OH-)+c(HA-)+c(A2-) |
6.下列各对物质中属于同分异构体的是( )
| A. | ${\;}_6^{12}$C与${\;}_6^{13}$C | B. | O2与O3 | ||
| C. |  与 与 | D. | 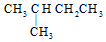 与 与 |
13.下列有机物中不能发生银镜反应的是( )
| A. | 麦芽糖 | B. | 乙酸 | C. | 甲酸甲酯 | D. | 乙醛 |
10.用石油和煤可以得到有机化工生产中需要的众多原料,例如由石油得到的乙烯和由煤得到的苯制聚苯乙烯.生产过程如下:
①CH2═CH2+ →
→
② $\stackrel{-H_{2}}{→}$
$\stackrel{-H_{2}}{→}$ 
③ →
→
下列说法不正确的是( )
①CH2═CH2+
 →
→
②
 $\stackrel{-H_{2}}{→}$
$\stackrel{-H_{2}}{→}$ 
③
 →
→
下列说法不正确的是( )
| A. | 通过裂解可以从石油中获得更多的乙烯 | |
| B. | 把煤干馏可以得到粗苯,经分馏可以得到苯 | |
| C. | 制聚苯乙烯的反应①为取代反应,②为消去反应③为加聚反应 | |
| D. | 反应①②③的原子利用率不都为100% |
5.某工厂对工业污泥中的Cr元素回收与再利用的工艺如图(已知硫酸浸取液中的金属离子主要是Cr3+,其次是少量的Fe2+、Fe3+、Al3+、Ca2+、Mg2+):

部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见表:
(1)实验室用98%(密度为1.84g•cm-3)的浓硫酸配制200mL 4.8mol•L-1的硫酸溶液,配制时需要量取98%的浓硫酸的体积为52.2 mL(保留小数点后一位小数),所用的玻璃仪器除烧杯、玻璃棒、量筒和酸式滴定管外,还需200mL容量瓶,胶头滴管.
(2)过滤操作时,需要对沉淀进行洗涤,洗漆沉淀的方法是沿玻璃棒向漏斗中注入蒸馏水,至刚好浸没沉淀物,等蒸馏水自然流尽后,再重复操作2到3次.
(3)加入H2O2的作用一方面是氧化+3价Cr使之转变成+6价Cr(CrO42-或Cr2O72-),以便于与杂质离子分离:另一方面是2Fe2++H2O2+2H+=2Fe3++2H2O.(离子方程式表示)
(4)调节溶液的pH=8除去的杂质离子是Al3+、Fe3+.
(5)钠离子交换树脂的原理为:Mn++nNaR→MRn+nNa+,被交换的杂质离子是Ca2+、Mg2+.
(6)通SO2气体时,还原过程发生以下反应(填写缺项物质并配平):
Na2Cr2O7+3SO2+11H2O=2Cr(OH)(H2O)5SO4+1Na2SO4.

部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见表:
| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cr3+ |
| 开始沉淀时的pH | 1.9 | 7.0 | -- | -- | -- |
| 沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8 | 9(>9溶解) |
(2)过滤操作时,需要对沉淀进行洗涤,洗漆沉淀的方法是沿玻璃棒向漏斗中注入蒸馏水,至刚好浸没沉淀物,等蒸馏水自然流尽后,再重复操作2到3次.
(3)加入H2O2的作用一方面是氧化+3价Cr使之转变成+6价Cr(CrO42-或Cr2O72-),以便于与杂质离子分离:另一方面是2Fe2++H2O2+2H+=2Fe3++2H2O.(离子方程式表示)
(4)调节溶液的pH=8除去的杂质离子是Al3+、Fe3+.
(5)钠离子交换树脂的原理为:Mn++nNaR→MRn+nNa+,被交换的杂质离子是Ca2+、Mg2+.
(6)通SO2气体时,还原过程发生以下反应(填写缺项物质并配平):
Na2Cr2O7+3SO2+11H2O=2Cr(OH)(H2O)5SO4+1Na2SO4.