题目内容
X2、Y2、Z2三种单质常温下均为气体。X2在Z2中燃烧生成XZ,火焰呈苍白色;X2Y常温下为液体。下列说法正确的是( )
| A.Y2是氯气 |
| B.铁分别与Y2、Z2作用,可分别形成含+3、+2价铁的化合物 |
| C.Z2具有漂白性 |
| D.XZ溶液使紫色石蕊溶液变红,原因是XZ电离出X+ |
D
解析试题分析:X2、Y2、Z2三种单质常温下均为气体.X2在Z2中燃烧生成XZ,火焰呈苍白色,说明是氢气在氯气中燃烧.推断X为H2,Z为Cl2;X2Y常温下为液体推断为H2O,Y2为O2;A、根据推断可知Y2为O2,故A错误;B、铁和Y2为O2反应可以形成+3价化合物,铁和Z为Cl2反应生成+3价化合物,故B错误;C、Z2为Cl2不具有漂白性,是氯气和水反应生成的次氯酸具有漂白作用,故C错误;D、XZ为HCl溶于水形成盐酸溶液使紫色石蕊溶液变红,原因是HCl电离出H+显酸性,故D正确;故选D。
考点:无机物的推断

 科学实验活动册系列答案
科学实验活动册系列答案下列实验“操作和现象”与“结论”对应关系正确的是( )
| | 操作和现象 | 结论 |
| A | 向NaCl溶液中先滴加少量AgNO3溶液,后滴加少量NaI溶液,先有白色沉淀,后变成黄色沉淀 | 说明Ksp(AgI)<Ksp (AgCl) |
| B | 将SO2通入酸性KMnO4溶液中,紫色褪去 | 说明SO2具有漂白性 |
| C | 向FeCl3和CuCl2混合溶液中加入铁粉,有红色固体析出 | 说明氧化性:Cu2+>Fe3+ |
| D | 向某溶液中先滴加硝酸酸化,再滴加BaCl2溶液,有白色沉淀生成 | 该溶液中一定含有Ag+ |
中学化学常见物质甲、乙、丙、丁之间存在转化关系:甲十乙 丙十丁。下列说法正确的是
丙十丁。下列说法正确的是
| A.若甲为钠单质,丁为氢气,则乙一定是水 |
| B.若甲为铝单质,丁为铁单质,则乙一定是氧化铁 |
| C.若甲为铜单质,丁为氯化亚铁溶液,则乙一定是氯化铁溶液 |
| D.若甲、乙、丙、丁均为化合物,则该反应一定属于复分解反应 |
下列推断合理的是
| A.金刚石是自然界中硬度最大的物质,不可能与氧气发生反应 |
| B.将SO2分别通入品红和溴水溶液,溶液都会褪色,而且再经加热都能恢复原色 |
| C.浓H2SO4,具有强氧化性,不能与Cu发生剧烈反应 |
| D.明矾[KAl(SO4)2·12H2O]在水中能形成Al(OH)3胶体,可用作净水剂 |
某装有红色溶液的试管,加热时溶液颜色逐渐变浅,则原溶液可能是( )
①滴有石蕊的盐酸溶液 ②滴有酚酞的氢氧化钠溶液 ③溶有SO2的品红溶液
④滴有酚酞的饱和氢氧化钙溶液 ⑤酚酞溶液中滴加少量NaClO溶液
| A.①④⑤ | B.①③ | C.③④⑤ | D.①④ |
下列装置或操作能达到实验目的的是 ( )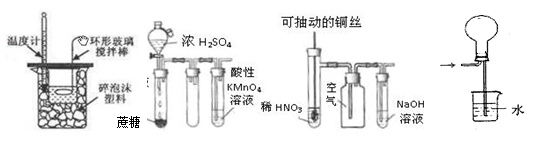
I II III IV
| A.实验I:中和热测定 |
| B.实验II:酸性KMnO4溶液中出现气泡,且颜色逐渐褪去 |
| C.实验III:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色 |
| D.实验IV:可用于HCl气体的吸收 |
下列叙述正确的是( )
①久置于空气中的氢氧化钠溶液,加足量盐酸时有气体产生②若R的含氧酸的酸性大于Q的含氧酸的酸性,则非金属性R大于Q③SiO2和CO2都是酸性氧化物,都能与强碱溶液反应,但不能与任何酸反应④玻璃、水泥、水晶项链都是硅酸盐制品⑤液态氟化氢中存在氢键,所以其分子比氯化氢更稳定⑥氢氧化铁胶体与氯化铁溶液分别蒸干灼烧得相同的物质
| A.①⑥ | B.①④⑥ | C.②③④ | D.④⑤⑥ |
下列实验的操作、现象和解释或结论都正确的是
| | 操 作 | 现 象 | 解释或结论 |
| A | 向装有Fe(NO3)2溶液的试管中加入几滴稀H2SO4 | 溶液颜色基本不变 | Fe(NO3)2与H2SO4不反应 |
| B | 向饱和Na2CO3溶液中通入足量CO2 | 溶液变浑浊 | 析出了NaHCO3晶体 |
| C | 向棕黄色的FeCl3溶液中加入足量的Mg粉 | 溶液变成浅绿色 | 2Fe3++Mg=2Fe2+ + Mg2+ |
| D | 将Na放入CuSO4溶液中 | 有红色固体析出 | 2Na+Cu2+=Cu+2Na+ |
下列判断错误的是
| A.非金属氧化物不一定是酸性氧化物,金属氧化物不一定为碱性氧化物 |
| B.联合制碱法在滤出NaHCO3后,为使滤液中NH4Cl析出更多更纯,通氨气加食盐冷却 |
| C.发生化学反应时失去电子数越多的金属原子,还原能力不一定越强 |
| D.氯水、Na2O2、活性炭都能使品红溶液褪色,但原理彼此都不相同 |