题目内容
(12分)已知氢氟酸、醋酸、氢氰酸(HCN)、碳酸在室温下的电离常数分别为:
根据上述数据,回答下列问题:
(1)四种酸中酸性最强的是_____________,四种酸中酸性最弱的是_____________。
(2)写出H2CO3电离方程式是 、 。
(3)写出反应的方程式:足量的氢氟酸与碳酸钠溶液混合:___________ ______,
足量的CO2通入NaCN溶液中:_________ _____。
| ① | HF | Ka=6.8×10-4 mol?L-1 |
| ② | CH3COOH | Ka=1.7×10-5 mol?L-1 |
| ③ | HCN | Ka=6.2×10-10 mol?L-1 |
| ④ | H2CO3 | Ka1=4.4×10-7mol?L-1 Ka2=4.7×10-11 mol?L-1 |
(1)四种酸中酸性最强的是_____________,四种酸中酸性最弱的是_____________。
(2)写出H2CO3电离方程式是 、 。
(3)写出反应的方程式:足量的氢氟酸与碳酸钠溶液混合:___________ ______,
足量的CO2通入NaCN溶液中:_________ _____。
(1)氢氟酸, HCN
(2)H2CO3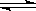 HCO3—+H+, HCO3—
HCO3—+H+, HCO3—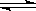 CO32—+H+
CO32—+H+
( 3)2HF+Na2CO3=2NaF+H2O+CO2↑, NaCN+H2O+CO2= HCN+NaHCO3
(2)H2CO3
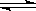 HCO3—+H+, HCO3—
HCO3—+H+, HCO3—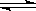 CO32—+H+
CO32—+H+( 3)2HF+Na2CO3=2NaF+H2O+CO2↑, NaCN+H2O+CO2= HCN+NaHCO3
(1)电离常数越大,相应酸的酸性越强,所以根据电离常数可知,酸性最强的是氢氟酸,而最弱的是HCN。
(2)碳酸是二元弱酸,电离是分步进行的,所以电离方程式依次是
H2CO3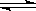 HCO3—+H+、HCO3—
HCO3—+H+、HCO3—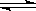 CO32—+H+。
CO32—+H+。
(3)由于氢氟酸的电离常数大于碳酸的电离常数,所以根据较强酸制取较弱的酸可知,反应的方程式是2HF+Na2CO3=2NaF+H2O+CO2↑;由于碳酸的第一步电离常数大于HCN的,但第二步小于HCN的,所以足量的CO2通入NaCN溶液中反应方程式是NaCN+H2O+CO2= HCN+NaHCO3。
(2)碳酸是二元弱酸,电离是分步进行的,所以电离方程式依次是
H2CO3
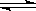 HCO3—+H+、HCO3—
HCO3—+H+、HCO3—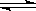 CO32—+H+。
CO32—+H+。(3)由于氢氟酸的电离常数大于碳酸的电离常数,所以根据较强酸制取较弱的酸可知,反应的方程式是2HF+Na2CO3=2NaF+H2O+CO2↑;由于碳酸的第一步电离常数大于HCN的,但第二步小于HCN的,所以足量的CO2通入NaCN溶液中反应方程式是NaCN+H2O+CO2= HCN+NaHCO3。

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案 走进文言文系列答案
走进文言文系列答案
相关题目
 变化的曲线如图所示。据图判断正确的是( )
变化的曲线如图所示。据图判断正确的是( )