题目内容
工业上通常以铝土矿(主要成分为Al2O3)为原料制备无水氯化铝:2Al2O3+6Cl2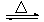 4AlCl3+3O2 ↑。请回答下列问题:
4AlCl3+3O2 ↑。请回答下列问题:
(1)上述反应涉及的元素中,最外层有2个未成对电子的元素是__________;简单离子的离子半径最小的元素,其原子核外有_____种不同能级的电子。
(2)已知元素周期表中,镓(31Ga)与铝元素同一主族,写出Ga的最外层电子排布式:______
(3)镓(Ga)有两种天然同位素,一种是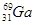 ,其原子在天然同位素原子中所占的百分比为60%。实验测得溴化镓(GaBr3)的摩尔质量为309.8 g/mol,则由此推知镓的另一种同位素是_________。
,其原子在天然同位素原子中所占的百分比为60%。实验测得溴化镓(GaBr3)的摩尔质量为309.8 g/mol,则由此推知镓的另一种同位素是_________。
(4)为促进反应的进行,实际生产中需加入焦炭,其原因是 。
 4AlCl3+3O2 ↑。请回答下列问题:
4AlCl3+3O2 ↑。请回答下列问题:(1)上述反应涉及的元素中,最外层有2个未成对电子的元素是__________;简单离子的离子半径最小的元素,其原子核外有_____种不同能级的电子。
(2)已知元素周期表中,镓(31Ga)与铝元素同一主族,写出Ga的最外层电子排布式:______
(3)镓(Ga)有两种天然同位素,一种是
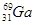 ,其原子在天然同位素原子中所占的百分比为60%。实验测得溴化镓(GaBr3)的摩尔质量为309.8 g/mol,则由此推知镓的另一种同位素是_________。
,其原子在天然同位素原子中所占的百分比为60%。实验测得溴化镓(GaBr3)的摩尔质量为309.8 g/mol,则由此推知镓的另一种同位素是_________。(4)为促进反应的进行,实际生产中需加入焦炭,其原因是 。
(1)氧(O) ;5 (各1分,共2分)
(2)4s24p 1 (2分)
(3)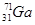 (2分)
(2分)
(4)碳与O2反应,有利于反应正向进行 (2分)
(2)4s24p 1 (2分)
(3)
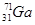 (2分)
(2分)(4)碳与O2反应,有利于反应正向进行 (2分)
试题分析:(1)Al、O、Cl元素原子外围电子排布分别为为3s23p1、2s22p4、3s23p5,故氧元素原子最外层有2个未成对电子。电子层数越多微粒半径越大,在核外电子排布相同的条件下,核电荷数越多,微粒半径越小,所以简单离子的离子半径最小的元素为Al元素,核外电子排布式为1s22s22p63s23p1,核外有5种不同能级的电子。
(2)镓(31Ga)与铝元素同一主族,铝的原子序数是13,因此镓7元素的原子序数是13+18=31,处于第四周期,最外层电子数为3,所以Ga的最外层电子排布式为4s24p1。
(3)溴化镓(GaBr3)的摩尔质量309.8g/mol,则镓元素的相对原子质量为309.8-80×3=69.8。设镓的另一种同位素的质量数为A,则根据元素原子所占的百分比可知,0.4A+0.6×69=69.8,解得A=71,故该同位素为
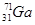
(4)实际生成中加入焦炭,碳与O2反应,降低氧气的浓度,有利于反应正向进行。

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案
相关题目
