��Ŀ����
��1 mol ��þ���ʵ�������Ϊa��þ���Ͻ����ں���b mol HNO3��ϡ��Һ�У��պ���ȫ��Ӧ��NOΪΨһ��ԭ�����������Һ����μ���NaOH��Һ���������ټ���Ϊֹ�������ó������ˡ�ϴ�������������أ����ù���������ԭ�Ͻ�������ȡ�����˵������ȷ����
�ٺϽ�þ��������Ϊ60%�ڷ�Ӧ�зų���������ڱ�״����Ϊ��1��a/3���� 22.4 L�۷�Ӧ����������������Ϊ��78��20a��g�ܷ�Ӧ�й�����NaOH��b����1��a/3����mol
A���٢ڢ� B���٢ڢܡ����� C���٢ۢ� D���ڢۢ�
A
����:

��14�֣��о�CO2�����öԴٽ���̼���Ĺ���������Ҫ�����塣
��1����֪ʯī�ı�ȼ����Ϊy kJ��mol��1��1.2gʯī��1.68L����״����������ȼ�գ�����Ӧ��ľ����ų�x kJ��������ʯī��������Ӧ����CO���Ȼ�ѧ����ʽΪ ��
��2������ʱ����CO��ԭMgSO4���Ʊ��ߴ�MgO��
��750��ʱ����������к������ʵ���SO2��SO3����ʱ��Ӧ�Ļ�ѧ����ʽ�� ��
����MgO���Ƴɡ�þ���������Ρ�ȼ�ϵ�أ���װ��ʾ��ͼ��ͼ1���õ�ط�Ӧ�����ӷ���ʽΪ �� 
 ��
�� 
ͼ1 ͼ2 ͼ3
��3��������̼�ϳɼ״���̼���ŵ��·���CO2ת��Ϊ�״����Ȼ�ѧ����ʽΪ��
CO2(g) +3H2(g)  CH3OH(g) +H2O(g) ��H
CH3OH(g) +H2O(g) ��H
�ٸ÷�Ӧ��ƽ�ⳣ������ʽΪK= ��
��ȡ��ݵ����CO2��H2�Ļ������(���ʵ���֮�Ⱦ�Ϊ1��3)���ֱ�����¶Ȳ�ͬ���ݻ���ͬ�ĺ����ܱ������У�����������Ӧ����Ӧ��ͬʱ���ü״������������(CH3OH)�뷴Ӧ�¶�T�Ĺ�ϵ������ͼ2��ʾ��������CO2ת��Ϊ�״���Ӧ�Ħ�H (�>�� ��<������)0��
�������ֲ�ͬ�����·�����Ӧ�����CH3OH�����ʵ�����ʱ��仯��ͼ3��ʾ������I�����Ӧ��ƽ�ⳣ����С��ϵΪK�� K��(�>�� ��<������)��
��һ���¶��£����ݻ���ͬ�ҹ̶��������ܱ������У������·�ʽͶ�뷴Ӧ�һ��ʱ���ﵽƽ�⡣
| �� �� | �� | �� |
| ��Ӧ�� Ͷ���� | 1molCO2 3molH2 | a molCO2��b molH2�� c molCH3OH(g)��c molH2O(g) |
������ƽ��������ѹǿΪ��ʼʱ��0.8����Ҫʹƽ������������ͬ��ֵ����������ȣ�����ʼʱά�ַ�Ӧ������У���c��ȡֵ��ΧΪ ��

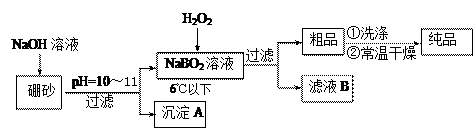
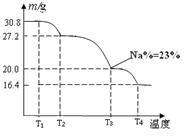
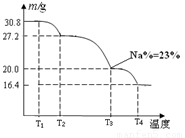
 ���н�����NaBO2 �����Ʒ���Ƶ��������� �� ���� �����ߡ��������͡����䡱����[��Դ:ѧ����ZXXK]
���н�����NaBO2 �����Ʒ���Ƶ��������� �� ���� �����ߡ��������͡����䡱����[��Դ:ѧ����ZXXK]
 (2)þ���Ͻ�(Mg17Al12 )��һ��DZ�ڵ�������ϣ�������������£���һ����ѧ�����ȵ�Mg��Al ������һ���¶���������á��úϽ���һ����������ȫ����ķ�Ӧ����ʽΪMg17Al122+17H2=17MgH2+12Al���õ��Ļ����Y(17MgH2 +12Al)��һ�������¿��ͷų�������
(2)þ���Ͻ�(Mg17Al12 )��һ��DZ�ڵ�������ϣ�������������£���һ����ѧ�����ȵ�Mg��Al ������һ���¶���������á��úϽ���һ����������ȫ����ķ�Ӧ����ʽΪMg17Al122+17H2=17MgH2+12Al���õ��Ļ����Y(17MgH2 +12Al)��һ�������¿��ͷų�������  ����0. 5 mol��L-1 NaOH ��1. 0 mol��L-1 MgCl2��Һ�У� ͼ8
����0. 5 mol��L-1 NaOH ��1. 0 mol��L-1 MgCl2��Һ�У� ͼ8