题目内容
【题目】工业上利用CO和H2合成甲醇,而CO和H2来源于煤的气化。回答下列问题。
(I).(1)己知:①H2(g)+1/2O2(g)=H2O(g) △H1=-241.8kJ/mol
②C(s)+ ![]() O2(g)=CO(g) △H2=-110.5kJ/mol
O2(g)=CO(g) △H2=-110.5kJ/mol
则焦炭与水蒸气反应的热化学方程式为_____________。
(2)已知反应CO(g)+2H2(g)![]() CH3OH(g) △H=-99kJ/mol中的相关化学键键能如下:
CH3OH(g) △H=-99kJ/mol中的相关化学键键能如下:
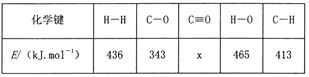
则x=________
(II)(3)在一容积可变的密闭容器中,lmolCO与2molH2发生反应:CO(g)+2H2(g) ![]() CH3OH(g), CO在不同温度下的平衡转化率(a)与总压强的关系如下图所示。
CH3OH(g), CO在不同温度下的平衡转化率(a)与总压强的关系如下图所示。
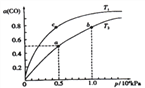
①该反应的△S_____0,图中的Tl____T2(填“>”、“<”或“=”)。
②该合成反应的温度一般控制在240~270℃,选择此温度范围的原因有:________。
③图中a点时以CH3OH的物质的量分数为_______,该反应的压强平衡常数为Kp=______(KPa)-2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4)利用合成气(主要成分为CO和H2)合成甲醇,发生主要反应如下:
I: CO(g)+2H2(g) ![]() CH3OH(g) △H1
CH3OH(g) △H1
II:CO2(g)+H2(g) ![]() CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2
III:CO2(g)+3H2(g) ![]() CH3OH(g) +H2O(g) △H31
CH3OH(g) +H2O(g) △H31
上述反应对应的平衡常数分别为K1、K2、K3,它们随温度变化曲线如下图所示。

则△H1______△H3(填“>”、“<”或“=”)。理由是____________。
【答案】 C(s)+H2O(g)===CO(g) + H2 (g) △H2=+131. 3 kJ/mol 1076 < < 此温度范围下的催化剂活性高;温度低于240℃,反应速率太慢;同时该反应为放热反应,温度高于270℃,化学平衡逆向移动,转化率降低 0.25 1.6×10-7 < 由图可知,随着温度升高,K2减小,则△H2>0,根据盖斯定律又得△H3=△H1+△H2,所以△H1<△H3(1分)
【解析】(I)(1)己知:①H2(g)+1/2O2(g)=H2O(g) △H1=-241.8kJ/mol,
②C(s)+ ![]() O2(g)=CO(g) △H2=-110.5kJ/mol,根据盖斯定律可知由②-①可得C(s)+H2O(g)===CO(g) + H2 (g) ,则△H2=(-110.5kJ/mol)-(-241.8kJ/mol)=+131. 3 kJ/mol ;即焦炭与水蒸气反应的热化学方程式为C(s)+H2O(g)===CO(g) + H2 (g) △H2=+131. 3 kJ/mol ;
O2(g)=CO(g) △H2=-110.5kJ/mol,根据盖斯定律可知由②-①可得C(s)+H2O(g)===CO(g) + H2 (g) ,则△H2=(-110.5kJ/mol)-(-241.8kJ/mol)=+131. 3 kJ/mol ;即焦炭与水蒸气反应的热化学方程式为C(s)+H2O(g)===CO(g) + H2 (g) △H2=+131. 3 kJ/mol ;
(2)反应焓变=反应物键能总和-生成物键能总和,即CO(g)+2H2(g)CH3OH(g),x+2×436-413×3-343-465=-99,解之得x=1076;
(II)①反应CO(g)+2H2(g) ![]() CH3OH(g)正方向是气体物质的量总和减小的方向,则△S<0,压强相同时一氧化碳的转化率高,所以平衡正向移动,而正反应是放热反应,温度升高,平衡逆向移动,CO的平衡转化率减小,故Tl<T2;
CH3OH(g)正方向是气体物质的量总和减小的方向,则△S<0,压强相同时一氧化碳的转化率高,所以平衡正向移动,而正反应是放热反应,温度升高,平衡逆向移动,CO的平衡转化率减小,故Tl<T2;
②当温度低于240℃,反应速率太慢;同时该反应为放热反应,温度高于270℃,化学平衡逆向移动,转化率降低,可见该合成反应的温度一般控制在240~270℃,并且此时催化剂活性高;
③a点的一氧化碳转化率为50%,总压为0.5MPa,
CO(g)+2H2(g)CH3OH(g)
起始量(mol)12 0
变化量(mol)x2xx
平衡量(mol)1-x2-2x x
而一氧化碳转化率为50%,所以x=0.5mol,a点时以CH3OH的物质的量分数为![]() ×100%=25%;Kp=
×100%=25%;Kp=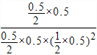 =1.6×10-7(kPa)-2;
=1.6×10-7(kPa)-2;
(4)由图可知,随着温度升高,K2减小,则△H2>0,根据盖斯定律又得△H3=△H1+△H2,所以△H1<△H3。

 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案【题目】某兴趣小组同学对实验室制备氧气的条件进行如下探究。
【提出问题】①氧化铜是否也能做氯酸钾分解的催化剂?它是否比二氧化锰催化效果好?
【查阅资料】研究表明,许多金属氧化物对氯酸钾的分解有催化作用。分别用下列金属氧化物作催化剂,氯酸钾开始发生分解反应和反应剧烈时的温度如下表所示:
催化剂 温度 反应程度 | 氧化铁 | 氧化铝 | 氧化铜 | 氧化镁 |
开始反应 | 420℃ | 515℃ | 305℃ | 490℃ |
剧烈反应 | 490℃ | 540℃ | 350℃ | 545℃ |
实验室用氯酸钾制取氧气,如果不用二氧化锰作催化剂,最好选用的金属氧化物是___________。
【设计并完成实验】
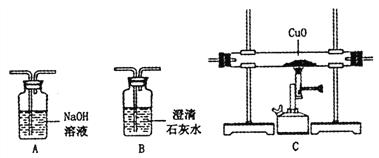
Ⅰ. 将3.0g氯酸钾放在试管中加热
Ⅱ. 将3.0g氯酸钾与1.0g二氧化锰均匀混合加热
Ⅲ. 将3.0g氯酸钾与Xg氧化铜均匀混合加热
【实验现象分析】
Ⅲ中X的值应为_____________,实验Ⅰ和Ⅲ比较可证明______________________。 现象与实验Ⅲ相同.实验Ⅱ和Ⅲ对比的目的是______________________。将实验Ⅲ反应后的固体加水溶解、过滤、洗涤、干燥,然后进行称量的目的是_____________________________,最后还要再将黑色粉末和_______________混合加热进行实验。
【结论】氧化铜也能作氯酸钾分解的催化剂,实验Ⅲ中的化学反应的化学方程式为_____________________________________________________。
【实验反思】MnO2的用量对 H2O2分解反应有何影响?
【设计并完成实验】利用图甲装置探究“MnO2的用量对 H2O2分解反应的影响”,实验中为3% H2O2溶液,装置中产生氧气的量可以用压强传感器测出(在等温条件下,产生氧气体积与装置内压强成正比,反应放热忽略不计。)
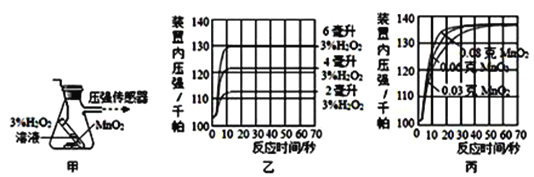
【讨论交流】(1)图乙是“0.1克MnO2与不同体积的3%H2O2溶液混合”的实验结果,从图中可以看出________________________________。图丙是“不同质量的MnO2与相同体积的3%H2O2溶液混合”的实验结果,从图中可以看出____________________________________。
【题目】近现代中国科学家在化学领域取得了卓越的成就,下列过程不涉及化学变化的是
侯氏制碱法 | 人工合成牛胰岛素 | 用青蒿素治疗疟疾 | 独创无氰电镀新工艺 |
|
|
|
|
A.以NH3、CO2、NaCl为原料最终制得纯碱 | B.由有机小分子合成有机高分子 | C.用萃取原理从青蒿中提取青蒿素 | D.以铜盐、碱等溶液为电解液镀铜 |
A. A B. B C. C D. D