题目内容
【题目】下列分子的空间构型可用sp2杂化轨道来解释的是( )
①BF3 ②  ③
③ ④C2H2 ⑤N2H4 ⑥C6H6
④C2H2 ⑤N2H4 ⑥C6H6
A. ①②③ B. ①②⑥ C. ②③⑤ D. ③④⑥
【答案】B
【解析】
根据杂化轨道数判断杂化类型,杂化轨道数=δ键数+孤对电子对数,据此判断杂化类型。
①BF3分子中硼原子杂化轨道数为3,所以采取sp2杂化,故正确;
②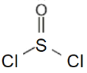 分子中硫原子杂化轨道数为3,所以采取sp2杂化,故正确;
分子中硫原子杂化轨道数为3,所以采取sp2杂化,故正确;
③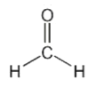 分子中硫原子杂化轨道数为3,所以采取sp2杂化,故正确;
分子中硫原子杂化轨道数为3,所以采取sp2杂化,故正确;
④CH≡CH分子中每个碳原子杂化轨道数为2,所以采取sp杂化,故错误;
⑤N2H4分子中每个氮原子杂化轨道数为4,所以采取sp3杂化,故错误;
⑥C6H6分子中碳原子杂化轨道数为3,所以采取sp2杂化,故正确;
综上所述,本题选B。

练习册系列答案
相关题目
