题目内容
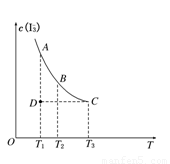
实验室将I2溶于KI溶液中,配制浓度较大的碘水,主要是因为发生了反应:I2(aq)+I-(aq) I3- (aq)。上述平衡体系中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上的任何一点都表示平衡状态)。下列说法不正确的是
A.该反应的正反应是吸热反应
B.A点与C点的化学反应速率vA<vC
C.反应进行到D点时,v(正)>v(逆)
D.A点与B点相比,B点的c(I-)大
A
解析:由图像可知温度越高生成物的浓度越低,因此正反应是放热反应。C点的温度高于A点的,因此C点反应速率大。D点要想达到平衡状态,在温度不变的情况下,要到达A点,而在这个变化过程中,生成物的浓度是增大的,即反应向正反应方向进行,即正反应速率大于逆反应速率。B点温度高,有利于反应向逆反应方向移动,故B点c(I-)大,答案选A。

练习册系列答案
 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
实验室将I2溶于KI溶液中,配制浓度较大的碘水,主要是因为发生了反应:I2(aq)+I-(aq) I(aq),上述平衡体系中,I的物质的量浓度c(I)与温度T的关系如图所示(曲线上的任何一点都表示平衡状态),不正确的是( )
I(aq),上述平衡体系中,I的物质的量浓度c(I)与温度T的关系如图所示(曲线上的任何一点都表示平衡状态),不正确的是( ) 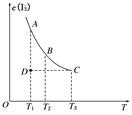
| A.该反应的正反应是吸热反应 | B.在反应进行到D点时,v正>v逆 |
| C.A点与C点的化学反应速率vA<vC | D.A点与B点相比,B点的c(I2)大 |
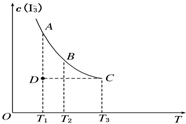 实验室将I2溶于KI溶液中,配制浓度较大的碘水,主要是因为发生了反应:I2(aq)+I-(aq)?I
实验室将I2溶于KI溶液中,配制浓度较大的碘水,主要是因为发生了反应:I2(aq)+I-(aq)?I I(aq),上述平衡体系中,I的物质的量浓度c(I)与温度T的关系如图所示(曲线上的任何一点都表示平衡状态),不正确的是(
)
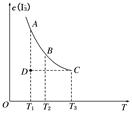
I(aq),上述平衡体系中,I的物质的量浓度c(I)与温度T的关系如图所示(曲线上的任何一点都表示平衡状态),不正确的是(
) 
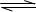 I2(aq)+I-(aq)
I3-(aq),上述平衡体系中,I3-的物质的量浓度c(I3-)与温度T的关系如右图所示(曲线上的任何一点都表示平衡状态)。下列说法不正确的是
(
)
I2(aq)+I-(aq)
I3-(aq),上述平衡体系中,I3-的物质的量浓度c(I3-)与温度T的关系如右图所示(曲线上的任何一点都表示平衡状态)。下列说法不正确的是
(
)
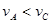
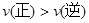
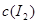 大
大 I(aq),上述平衡体系中,I的物质的量浓度c(I)与温度T的关系如图所示(曲线上的任何一点都表示平衡状态),下列说法不正确的是
I(aq),上述平衡体系中,I的物质的量浓度c(I)与温度T的关系如图所示(曲线上的任何一点都表示平衡状态),下列说法不正确的是