��Ŀ����
�����£���������Һ�з������·�Ӧ
��16H++10Z-+2XO4-��2X2++5Z2+8H2O ��2A2+ +B2��2A3++2B-
��2B-+Z2��B2+2Z-
�ɴ��ж�����˵��������ǣ� ��
��16H++10Z-+2XO4-��2X2++5Z2+8H2O ��2A2+ +B2��2A3++2B-
��2B-+Z2��B2+2Z-
�ɴ��ж�����˵��������ǣ� ��
| A����ӦZ2+2A2+��2A3++2Z-���Խ��С� |
| B����ԭ����ǿ������˳����A2+��B-��Z-��X2+ |
| C����������ǿ������˳����XO4-��Z2��B2��A3+ |
| D��ZԪ���ڢ٢۷�Ӧ�о�����ԭ |
D
���������A�����ݷ�Ӧ2A2��+B2=2A3��+2B�����ɵ���������B2��A3����2B��+Z2=B2+2Z�����ɵ���������Z2��B2��A3������ӦZ2+2A2��=2A3��+2Z�����Խ��У���A��ȷ��B��������ԭ��Ӧ�У���ԭ���Ļ�ԭ��ǿ�ڻ�ԭ����Ļ�ԭ�ԣ���Ӧ��16H��+10Z��+2XO4��=2X2��+5Z2+8H2O�У���ԭ��Z����X2������Ӧ��2A2��+B2=2A3��+2B���У���ԭ��A2����B������Ӧ��2B��+Z2=B2+2Z���У���ԭ��B����Z�������Ի�ԭ����ǿ������˳����A2����B����Z����X2������B��ȷ��C��������ԭ��Ӧ����������������ǿ����������������ԣ�����Ӧ��16H��+10Z��+2XO4��=2X2��+5Z2+8H2O�У�������XO4����Z2����Ӧ��2A2��+B2=2A3��+2B���У�������B2��A3������Ӧ��2B��+Z2=B2+2Z���У�������Z2��B2��������������ǿ������˳����XO4����Z2��B2��A3������C��ȷ��D��ZԪ���ڢ��л��ϼ����ߣ��ڷ�Ӧ�б��������ڢ��л��ϼ۽��ͣ��ڷ�Ӧ�б���ԭ����D����ѡD��

��ϰ��ϵ�д�
�����Ŀ

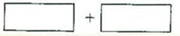
 AsO43-+2I-+ 2H2O���ڽ�ǿ����ʱ������������ԭ��Ӧ��____���У��������Ӧ�����淴Ӧ������ǿ����ʱ���Ƿ�����H3As3��ԭI2��Ϊʲô��_______________________________________��
AsO43-+2I-+ 2H2O���ڽ�ǿ����ʱ������������ԭ��Ӧ��____���У��������Ӧ�����淴Ӧ������ǿ����ʱ���Ƿ�����H3As3��ԭI2��Ϊʲô��_______________________________________��