题目内容
水煤气 (主要成分:CO、H2 ) 是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:
C (s) + H2O(g) ![]() CO (g) +H2 (g);△H =+131.3kJ•mol-1
CO (g) +H2 (g);△H =+131.3kJ•mol-1
(1)某温度下,四个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示。请填写表中相应的空格。
| 容器 编号 | c(H2O)/mol?L-1 | c(CO)/mol?L-1 | c(H2)/mol?L-1 | V正、V逆比较 |
| I | 0.06 | 0.60 | 0.10 | V正=V逆 |
| II | 0.06 | 0.50 | 0.40 | ? |
| III | 0.12 | 0.40 | 0.80 | V正<V逆 |
| IV | 0.12 | 0.30 | ? | V正=V逆 |
(2)另有一个容积可变的密闭容器。恒温恒压下,向其中加入1.0mol炭和 1.0mo l水蒸气 (H216O),发生上述反应,达到平衡时,容器的体积变为原来的1.25 倍。平衡时水蒸气的转化率为 ;向该容器中补充 a mol 炭,水蒸气的转化率将 (填 “增大”、“减小”、“不变”),再补充 a mol 水蒸气 (H218O), 最终容器中C16O和C18O 的物质的量之比为 。
(3)已知:C (s) + ![]() O2(g)=CO (g);△H = -110.5kJ?mo1-1
O2(g)=CO (g);△H = -110.5kJ?mo1-1
CO(g) + ![]() O2(g) =CO2 (g);△H =-283.0 kJ?mo1-1
O2(g) =CO2 (g);△H =-283.0 kJ?mo1-1
H2 (g) + ![]() O2 (g) =H2O (g);△H = -241.8kJ?mo1-1
O2 (g) =H2O (g);△H = -241.8kJ?mo1-1
那么,将2.4 g 炭完全转化为水煤气,然后再燃烧,整个过程△H = kJ?mo1-1
(1)
| V正 < V逆 | ||||
| 0.40 |
(2)25%;不变;1:a;
(3)-78.7

(本题15分)水煤气 (主要成分:CO、H2 ) 是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:
![]() C (s) + H2O(g)
C (s) + H2O(g)![]() CO (g) +H2 (g);△H =+131.3kJ•mol-1
CO (g) +H2 (g);△H =+131.3kJ•mol-1
![]() (1)某温度下,四个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示。请填写表中相应的空格。
(1)某温度下,四个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示。请填写表中相应的空格。
容器编号 | c(H2O)/mol?L-1 | c(CO)/mol?L-1 | c(H2)/mol?L-1 | V正、V逆比较 |
I | 0.06 | 0.60 | 0.10 | V正=V逆 |
II | 0.06 | 0.50 | 0.40 | ? |
III | 0.12 | 0.40 | 0.80 | V正<V逆 |
IV | 0.12 | 0.30 | ? | V正=V逆 |
(2)另有一个容积可变的密闭容器。恒温恒压下,向其中加入1.0mol炭和 1.0mo l水蒸气 (H216O),发生上述反应,达到平衡时,容器的体积变为原来的1.25 倍。平衡时水蒸气的转化率为 ;向该容器中补充 a mol 炭,水蒸气的转化率将 (填 “增大”、“减小”、“不变”),再补充 a mol 水蒸气 (H218O), 最终容器中C16O和C18O 的物质的量之比为 。
![]() (3)己知:C (s) +
(3)己知:C (s) + ![]() O2(g)=CO (g);△H = -110.5kJ?mo1-1
O2(g)=CO (g);△H = -110.5kJ?mo1-1
![]() CO(g) +
CO(g) + ![]() O2(g) =CO2 (g);△H =-283.0 kJ?mo1-1
O2(g) =CO2 (g);△H =-283.0 kJ?mo1-1
![]() H2 (g) +
H2 (g) + ![]() O2 (g) =H2O (g);△H = -241.8kJ?mo1-1
O2 (g) =H2O (g);△H = -241.8kJ?mo1-1
![]() 那么,将2.4 g 炭完全转化为水煤气,然后再燃烧,整个过程△H = kJ?mo1-1
那么,将2.4 g 炭完全转化为水煤气,然后再燃烧,整个过程△H = kJ?mo1-1
(7 分 )水煤气 (主要成分:CO、H2 ) 是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:
C (s) + H2O(g)≒CO(g) +H2 (g);△H =+131.3kJ•mol-1
(1)某温度下,四个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示。请填写表中相应的空格。
| 容器编号 | c(H2O)/mol·L-1 | c(CO)/mol·L-1 | c(H2)/mol·L-1 | V正、V逆比较 |
| I | 0.06 | 0.60 | 0.10 | V正=V逆 |
| II | 0.06 | 0.50 | 0.40 | ? |
| III | 0.12 | 0.40 | 0.80 | V正<V逆 |
| IV | 0.12 | 0.30 | ? | V正=V逆 |
(2)另有一个容积可变的密闭容器。恒温恒压下,向其中加入1.0mol炭和 1.0mo l水蒸气(H216O),发生上述反应,达到平衡时,容器的体积变为原来的1.25倍。平衡时水蒸气的转化率为 ;向该容器中补充 a mol 炭,水蒸气的转化率将 (填 “增大”、“减小”、“不变”),再补充 a mol 水蒸气 (H218O), 最终容器中C16O和C18O 的物质的量之比为 。
(3)己知:C (s) + ![]() O2(g)=CO(g);△H = -110.5kJ·mo1-1
O2(g)=CO(g);△H = -110.5kJ·mo1-1
CO(g) + ![]() O2(g)=CO2 (g);△H =-283.0 kJ·mo1-1
O2(g)=CO2 (g);△H =-283.0 kJ·mo1-1
H2 (g) + ![]() O2(g) =H2O (g);△H = -241.8kJ·mo1-1
O2(g) =H2O (g);△H = -241.8kJ·mo1-1
那么,将2.4 g 炭完全转化为水煤气,然后再燃烧,整个过程△H = kJ·mo1-1
(7 分 )水煤气 (主要成分:CO、H2 ) 是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:
C (s) + H2O(g)≒CO (g) +H2 (g);△H =+131.3kJ•mol-1
(1)某温度下,四个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示。请填写表中相应的空格。
|
容器编号 |
c(H2O)/mol·L-1 |
c(CO)/mol·L-1 |
c(H2)/mol·L-1 |
V正、V逆比较 |
|
I |
0.06 |
0.60 |
0.10 |
V正=V逆 |
|
II |
0.06 |
0.50 |
0.40 |
? |
|
III |
0.12 |
0.40 |
0.80 |
V正<V逆 |
|
IV |
0.12 |
0.30 |
? |
V正=V逆 |
(2)另有一个容积可变的密闭容器。恒温恒压下,向其中加入1.0mol炭和 1.0mo l水蒸气 (H216O),发生上述反应,达到平衡时,容器的体积变为原来的1.25 倍。平衡时水蒸气的转化率为 ;向该容器中补充 a mol 炭,水蒸气的转化率将 (填 “增大”、“减小”、“不变”),再补充 a mol 水蒸气 (H218O), 最终容器中C16O和C18O 的物质的量之比为 。
(3)己知:C (s) + 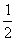 O2(g)=CO
(g);△H = -110.5kJ·mo1-1
O2(g)=CO
(g);△H = -110.5kJ·mo1-1
CO(g) + 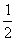 O2(g)
=CO2 (g);△H =-283.0 kJ·mo1-1
O2(g)
=CO2 (g);△H =-283.0 kJ·mo1-1
H2 (g) + 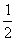 O2
(g) =H2O (g);△H = -241.8kJ·mo1-1
O2
(g) =H2O (g);△H = -241.8kJ·mo1-1
那么,将2.4 g 炭完全转化为水煤气,然后再燃烧,整个过程△H = kJ·mo1-1
 提取出来,经化学反应后使之变为可再生燃料甲醇。“绿色自由”构想技术流程如下:
提取出来,经化学反应后使之变为可再生燃料甲醇。“绿色自由”构想技术流程如下: