题目内容
元素A原子的L电子层比元素B原子的L电子层少3个电子,B元素原子核外总电子数比A元素原子核外总电子数多5个,则A、B可形成( )
A.离子化合物B2A3 B.离子化合物B3A2
C.共价化合物B2A3 D.共价化合物B3A2
A.离子化合物B2A3 B.离子化合物B3A2
C.共价化合物B2A3 D.共价化合物B3A2
B
L电子层上电子数A原子少,总电子数A原子也少,则A原子核电荷数少。由于A比B总电子数少5,而L层上只少3,这样K层上电子数一定相同,则M层还少2。所以A为氮元素,B为镁元素。Mg、N可形成Mg3N2,是离子化合物。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 量(q)有关,一般用偶极矩(μ)来衡量。分子的偶极矩定义为偶极长和偶极上一端电荷电量的乘积,即μ=d·q。试回答以下问题:
量(q)有关,一般用偶极矩(μ)来衡量。分子的偶极矩定义为偶极长和偶极上一端电荷电量的乘积,即μ=d·q。试回答以下问题: =1.03、μBCl3=0。由此可知,PF3分子是 构型,BCl3分子是 构型。
=1.03、μBCl3=0。由此可知,PF3分子是 构型,BCl3分子是 构型。 对物质的磁性研究表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是__________________。
对物质的磁性研究表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是__________________。 :在洁净铁(可用于合成氨
:在洁净铁(可用于合成氨
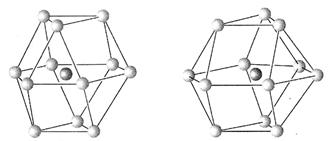
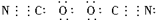 ,则SCN-的电子式正确的是( )
,则SCN-的电子式正确的是( )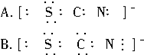
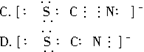
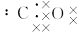 ,下列叙述,正确的是( )
,下列叙述,正确的是( )