题目内容
下列各项操作中不发生先沉淀后溶解现象的是
①向饱和Na2CO3溶液中通入过量CO2
②向Fe(OH)3胶体中逐滴滴入过量的H2SO4
③向AgI胶体中逐滴加入过量稀盐酸
④向石灰水中通入过量CO2
⑤向Na2SiO3溶液中滴入过量的盐酸.
- A.①②③
- B.②③⑤
- C.①②③⑤
- D.①③⑤
D
分析:①向饱和Na2CO3溶液中通入过量CO2生成NaHCO3比Na2CO3溶解度小;
②根据胶体的性质判断,加入稀硫酸产生聚沉现象,H2SO4与Fe(OH)3反应,所以出现先沉淀后溶解现象;
③根据胶体的性质判断,加入稀盐酸产生聚沉现象,AgCl与稀盐酸不反应;
④石灰水和CO2反应,生成CaCO3沉淀,继续通入CO2,会与CaCO3反应生成可溶的Ca(HCO3)2;
⑤生成硅酸沉淀.
解答:①中有Na2CO3+CO2+H2O=2NaHCO3,NaHCO3比Na2CO3溶解度小但质量大,且反应中中消耗H2O,故有沉淀析出且不溶解;②向Fe(OH)3胶体中加入H2SO4会出现先凝聚生成Fe(OH)3沉淀,H2SO4过量,Fe(OH)3与H2SO4反应而溶解;
③向AgI胶体中加入电解质HCl同样有沉淀,但不溶解;
④向石灰水中通CO2,反应有:Ca(OH)2+CO2=CaCO3+H2O; CaCO3+H2O+CO2=Ca(HCO3)2,现象为先沉淀后溶解;
⑤中生成硅酸沉淀,不溶解.
所以不溶解的是①③⑤.
故选D.
点评:本题考查较为综合,涉及元素化合物知识,胶体等,题目难度中等,解答本题的关键是把握物质的性质,注意胶体的性质.
分析:①向饱和Na2CO3溶液中通入过量CO2生成NaHCO3比Na2CO3溶解度小;
②根据胶体的性质判断,加入稀硫酸产生聚沉现象,H2SO4与Fe(OH)3反应,所以出现先沉淀后溶解现象;
③根据胶体的性质判断,加入稀盐酸产生聚沉现象,AgCl与稀盐酸不反应;
④石灰水和CO2反应,生成CaCO3沉淀,继续通入CO2,会与CaCO3反应生成可溶的Ca(HCO3)2;
⑤生成硅酸沉淀.
解答:①中有Na2CO3+CO2+H2O=2NaHCO3,NaHCO3比Na2CO3溶解度小但质量大,且反应中中消耗H2O,故有沉淀析出且不溶解;②向Fe(OH)3胶体中加入H2SO4会出现先凝聚生成Fe(OH)3沉淀,H2SO4过量,Fe(OH)3与H2SO4反应而溶解;
③向AgI胶体中加入电解质HCl同样有沉淀,但不溶解;
④向石灰水中通CO2,反应有:Ca(OH)2+CO2=CaCO3+H2O; CaCO3+H2O+CO2=Ca(HCO3)2,现象为先沉淀后溶解;
⑤中生成硅酸沉淀,不溶解.
所以不溶解的是①③⑤.
故选D.
点评:本题考查较为综合,涉及元素化合物知识,胶体等,题目难度中等,解答本题的关键是把握物质的性质,注意胶体的性质.

练习册系列答案
相关题目
 ② 向Fe(OH)3胶体中逐滴滴入过量的H2SO4溶液 ③ 向AgI胶体中逐滴加入过量稀盐酸
② 向Fe(OH)3胶体中逐滴滴入过量的H2SO4溶液 ③ 向AgI胶体中逐滴加入过量稀盐酸 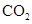 ②向
②向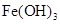 胶体中逐滴滴加人过量
胶体中逐滴滴加人过量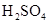 ③向
③向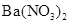 溶液中通人过量
溶液中通人过量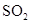 ④向石灰水中通人过量
④向石灰水中通人过量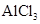 溶液中逐滴滴加NaOH溶液至过量
溶液中逐滴滴加NaOH溶液至过量