题目内容
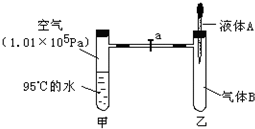 如图所示,活塞a开始时处于关闭状态,将液体A滴入试管乙中,与气体B充分反应后,打开活塞,可发现试管甲中的水立即沸腾了,则液体A和气体B的组合可能的是( )
如图所示,活塞a开始时处于关闭状态,将液体A滴入试管乙中,与气体B充分反应后,打开活塞,可发现试管甲中的水立即沸腾了,则液体A和气体B的组合可能的是( )| A、氢氧化钠溶液、一氧化氮 | B、水、二氧化碳 | C、氯化钠溶液、氨气 | D、新制氯水、甲烷 |
分析:水的沸点与压强有关,压强越小水的沸点越低,压强越大,水的沸点越高.
A.一氧化氮难溶于水,氢氧化钠与一氧化氮不反应,压强不会变化;
B.二氧化碳能溶于水,但1体积水中只能溶解1体积的二氧化碳,压强变化小;
C.氨气易溶于水,压强变化大;
D.甲烷和新制的氯水不反应,压强不会变化.
A.一氧化氮难溶于水,氢氧化钠与一氧化氮不反应,压强不会变化;
B.二氧化碳能溶于水,但1体积水中只能溶解1体积的二氧化碳,压强变化小;
C.氨气易溶于水,压强变化大;
D.甲烷和新制的氯水不反应,压强不会变化.
解答:解:A.氢氧化钠溶液不能吸收一氧化氮,打开活塞a甲中的压强不变,水的沸点不变,故A错误;
B.二氧化碳能溶于水,但1体积水中只能溶解1体积的二氧化碳,打开活塞a甲中的压强变化小,水的沸点降低小,不能沸腾,故B错误;
C.1体积水中能溶解700体积的氨气,打开活塞a甲中的压强减小,水的沸点降低,水沸腾了,故C正确;
D.甲烷和氯气在光照的条件下反应,甲烷和新制的氯水不反应,打开活塞a甲中的压强不变,水的沸点不变,故D错误;
故选C.
B.二氧化碳能溶于水,但1体积水中只能溶解1体积的二氧化碳,打开活塞a甲中的压强变化小,水的沸点降低小,不能沸腾,故B错误;
C.1体积水中能溶解700体积的氨气,打开活塞a甲中的压强减小,水的沸点降低,水沸腾了,故C正确;
D.甲烷和氯气在光照的条件下反应,甲烷和新制的氯水不反应,打开活塞a甲中的压强不变,水的沸点不变,故D错误;
故选C.
点评:本题以沸点的变化为载体考查了物质的性质,解答本题的关键是要充分理解水沸腾的原因,根据物质间反应后气体状态的改变,对问题做出正确的判断,题目难度不大.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
(12分).随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视。
(1)目前,用超临界CO2(其状态介于气态和液态之间)代替氟利昂作冷剂已成为一种趋势,这一做法对环境的积极意义在于 。
(2)将CO2转化成有机物可有效实现碳循环。CO2转化成有机物的例子很多,如:
以上反应中,最节能的是 ,原子利用率最高的是 。
(3)为探究用CO2来生产燃料甲醇的反应原理,现进行如下实验:
在体积为1L的密闭容器中,充入1molCO2和3molH2,一定条件下发生反应: CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H=-49.0kJ/mol
CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H=-49.0kJ/mol
测得CO2和CH3OH(g)的浓度随时间变化如图所示。
①从反应开始到平衡,氢气的平均反应速率v(H2)= mol/(L·min)
②该反应的平衡常数表达式为 ,升高温度,平衡常数的数值将
(填“增大”、“减小”或“不变”)。
③下列措施中能使n(CH3OH)/n(CO2)增大的是 .
| A.升高温度 | B.充入He(g),使体系压强增大 |
| C.将H2O(g)从体系中分离 | D.再充入1molCO2和3molH2 |

①当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如下图所示。

图t1时引起平衡移动的条件可能是 。
其中表示平衡混合物中NH3含量最高的一段时间是 。
②温度为T°C时,将3amolH2和amolN2放入带有活塞的密闭容器中,如果活塞能自由移动,充分反应后测得N2的转化率为50%。如果在相同温度下将3amolH2、amolN2和2amolNH3气体放入该容器中,平衡时H2的转化率为 。
 CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H=-49.0kJ/mol
CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H=-49.0kJ/mol 2Z(g)+W(g);ΔH>0。达平衡时,A的体积为1.2aL。下列说法错误的是
2Z(g)+W(g);ΔH>0。达平衡时,A的体积为1.2aL。下列说法错误的是
 2Z(g)+W(g);ΔH>0。达平衡时,A的体积为1.2aL。下列说法错误的是
2Z(g)+W(g);ΔH>0。达平衡时,A的体积为1.2aL。下列说法错误的是