题目内容
 实验室制乙烯的反应原理为CH3CH2OH
实验室制乙烯的反应原理为CH3CH2OH| 浓硫酸 | 170℃ |
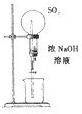
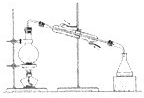
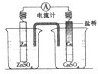
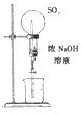
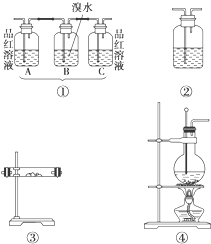
(1)请用图中编号为①、②、③、④的装置设计一个实验,以验证上述反应混合气体中含有CO2、SO2和水蒸气.用装置的编号表示装置的连接顺序(按产物气流从左到右):
④
④
→③
③
→①
①
→②
②
.(2)实验时装置①中A瓶的现象是
品红褪色
品红褪色
,原因是混合气中有SO2
混合气中有SO2
.B瓶中的现象是
橙色褪去
橙色褪去
;B瓶溶液的作用是除SO2气体
除SO2气体
.若C瓶中品红溶液不褪色,说明SO2被除尽
SO2被除尽
.(3)装置③中加的固体药品是
无水CuSO4
无水CuSO4
,以验证混合气体中有水蒸气
水蒸气
.装置②中盛的溶液是澄清石灰水
澄清石灰水
,以验证混合气体中的CO2
CO2
.(4)装置①在整套装置中所放位置的理由是
①要在③之后,否则气流会带出水蒸气,干扰水的检验;①要在②之前,否则SO2也会使石灰水变浑浊,干扰CO2的检验
①要在③之后,否则气流会带出水蒸气,干扰水的检验;①要在②之前,否则SO2也会使石灰水变浑浊,干扰CO2的检验
.分析:(1)检验二氧化硫用品红溶液,检验二氧化碳用澄清的石灰水,检验水蒸气用无水硫酸铜,因溶液中有水,所以首先检验水蒸气;因为CO2是用澄清石灰水来检验的,而SO2也可以使澄清石灰水变浑,二氧化硫能使品红褪色,二氧化碳不能,所以,检验二氧化硫在检验二氧化碳之前,再通过澄清石灰水确认CO2存在;
(2)二氧化硫能使品红褪色;SO2能和溴水发生氧化还原反应;
(3)无水硫酸铜和水作用,白色变蓝色;
(4)从干扰实验的角度进行分析解答;
(2)二氧化硫能使品红褪色;SO2能和溴水发生氧化还原反应;
(3)无水硫酸铜和水作用,白色变蓝色;
(4)从干扰实验的角度进行分析解答;
解答:解:(1)乙醇跟浓H2SO4温度过高反应,CH3CH2OH+4H2SO4(浓)
4SO2↑+CO2↑+7H2O+C,选用装置④;因溶液中有水,所以必须先检验水蒸气,选用装置③,放入无水硫酸铜,变蓝则说明有水生成;因二氧化碳和二氧化硫都能使澄清的石灰水变浑浊,二氧化硫能使品红褪色,二氧化碳不能,所以用装置①,A装置品红褪色,则说明有SO2气体产生,B装置吸收SO2,C装置品红不褪色,说明吸收完全;最后用装置②,通过澄清石灰水变浑浊,确认CO2存在,
故答案为:④③①②;
(2)实验时装置①的作用是检验二氧化硫的存在并除去二氧化硫,A瓶中装有品红溶液,二氧化硫能使品红褪色,所以现象是品红褪色,说明混合气中有SO2;B装置吸收SO2,SO2+Br2+2H2O=2H2SO4+2HBr,现象是橙色褪去;C装置品红不褪色,说明SO2吸收完全,
故答案为:品红褪色;混合气中有SO2;橙色褪去;除SO2气体;SO2被除尽;
(3)装置③的作用是检验水蒸气,用白色的无水硫酸铜粉末,CuSO4+5H2O═CuSO4?5H2O变蓝说明混合气体中有水蒸气;装置②的作用是检验二氧化碳,用澄清石灰水,Ca(OH)2+CO2=CaCO3↓+H2O,澄清石灰水变浑浊,确认CO2存在,
故答案为:无水CuSO4;水蒸气;澄清石灰水;CO2;
(4)因溶液中有水必须先检验水蒸气,所以①要在③之后,否则气流会带出水蒸气,干扰水的检验;二氧化碳和二氧化硫都能使澄清的石灰水变浑浊,二氧化硫能使品红褪色,二氧化碳不能,所以①要在②之前,
故答案为:①要在③之后,否则气流会带出水蒸气,干扰水的检验;①要在②之前,否则SO2也会使石灰水变浑浊,干扰CO2的检验;
| ||
故答案为:④③①②;
(2)实验时装置①的作用是检验二氧化硫的存在并除去二氧化硫,A瓶中装有品红溶液,二氧化硫能使品红褪色,所以现象是品红褪色,说明混合气中有SO2;B装置吸收SO2,SO2+Br2+2H2O=2H2SO4+2HBr,现象是橙色褪去;C装置品红不褪色,说明SO2吸收完全,
故答案为:品红褪色;混合气中有SO2;橙色褪去;除SO2气体;SO2被除尽;
(3)装置③的作用是检验水蒸气,用白色的无水硫酸铜粉末,CuSO4+5H2O═CuSO4?5H2O变蓝说明混合气体中有水蒸气;装置②的作用是检验二氧化碳,用澄清石灰水,Ca(OH)2+CO2=CaCO3↓+H2O,澄清石灰水变浑浊,确认CO2存在,
故答案为:无水CuSO4;水蒸气;澄清石灰水;CO2;
(4)因溶液中有水必须先检验水蒸气,所以①要在③之后,否则气流会带出水蒸气,干扰水的检验;二氧化碳和二氧化硫都能使澄清的石灰水变浑浊,二氧化硫能使品红褪色,二氧化碳不能,所以①要在②之前,
故答案为:①要在③之后,否则气流会带出水蒸气,干扰水的检验;①要在②之前,否则SO2也会使石灰水变浑浊,干扰CO2的检验;
点评:本题考查了乙醇跟浓硫酸反应生成二氧化硫、二氧化碳、水蒸气和炭黑产物的检验,注意当有多种产物需检验时,应考虑先后顺序,二氧化碳和二氧化硫都能使澄清的石灰水变浑浊,二氧化硫能使品红褪色,二氧化碳不能是解答本题的关键,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目