题目内容
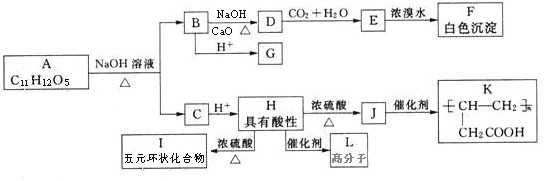
【题目】已知下图中A是固体单质,E是一种白色沉淀,F为密度最小的无色气体。且各种物质所含元素除H、O外,其余均为第三周期元素。

请按要求回答下列问题:
(1)若实现C→E转化所需的b溶液是“过量的盐酸”,则:B的化学式为__________________,C→E的离子方程式为__________________;
(2)若实现C→E转化所需的b溶液不能使用“过量的盐酸”,只能使用“少量的盐酸”则B的化学式为__________________,C→E的离子方程式为__________________;
(3)若实现C→E转化所需的b溶液是“过量的NaOH溶液”,则:E的化学式为__________________,反应B+a→C+D的离子方程式为__________________。
【答案】
(1)SiO2;SiO3 2- + 2H+ = H2SiO3↓;
(2)Al2O3;H++AlO2-+H2O=Al(OH)3↓;
(3)Mg(OH)2;MgO+2H+=Mg2++H2O。
【解析】
试题分析:A是一种固体单质,E是一种白色沉淀,F为密度最小的无色气体判断为H2.且各种物质所含元素除H、O外,其余均为第三周期元素,由反应转化关系可知E受热分解生成B+D;B为氧化物a溶液可以是酸溶液或碱溶液;b溶液可以对应是碱溶液或酸溶液;A+a=F+C是置换反应;
(1)b溶液是“过量的盐酸”,生成白色沉淀的物质为硅酸,C为硅酸盐,推断A为Si,B为SiO2,a溶液为强碱溶液如NaOH溶液;硅酸钠溶液中加入盐酸生成硅酸沉淀,C→E的离子方程式为SiO3 2- + 2H+ = H2SiO3↓,故答案为:SiO2;SiO3 2- + 2H+ = H2SiO3↓;
(2)实现C→E转化所需的b溶液为盐酸,但E能被过量的盐酸溶解,说明C为偏铝酸盐溶液,E为Al(OH)3;A为Al,B为Al2O3,a溶液为强碱溶液如NaOH;C→E的离子方程式为H++AlO2-+H2O=Al(OH)3↓;故答案为:H++AlO2-+H2O=Al(OH)3↓;
(3)若实现C→E转化所需的b溶液是“过量的NaOH溶液”,判断E沉淀可以是Mg(OH)2;A为Mg,B为MgO,C为Mg2+,D为H2O,F为Mg(OH)2;反应B+a→C+D的离子方程式为:MgO+2H+=Mg2++H2O,故答案为:Mg(OH)2;MgO+2H+=Mg2++H2O。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】根据金属活动性顺序表,Cu不能发生反应:Cu+2H2O= Cu(OH)2↓+H2↑。但选择恰当电极材料和电解液进行电解,这个反应就能变为现实。下列四组电极和电解液中,能实现该反应最为恰当的一组是
A | B | C | D | |
阳极 | 石墨棒 | Cu | Cu | Cu |
阴极 | 石墨棒 | Fe | 石墨棒 | Pt |
电解液 | CuSO4溶液 | H2SO4溶液 | Na2SO4溶液 | H2O |