题目内容
有X、Y、Z、V、W五种短周期元素,已知:
①Z+、V3+均与W的气态氢化物分子具有相同的电子数;X2-、Y-与Y的气态氢化物分子具有相同的电子数;
②X单质在空气中燃烧产生气体R;
③Y的气态氢化物与W的气态氢化物相遇时有白烟生成.
请回答:
(1)X2-的结构示意图为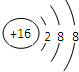
 .
.
(2)元素W在元素周期表中的位置是
(3)元素Z的单质在空气中燃烧产物的化学式为
(4)元素Z的最高价氧化物的水化物是一种强碱,写出元素V的单质与该强碱溶
反应的化学方程式
(5)向Y单质的水溶液中通入过量气体R的现象为
反应的离子方程式为
①Z+、V3+均与W的气态氢化物分子具有相同的电子数;X2-、Y-与Y的气态氢化物分子具有相同的电子数;
②X单质在空气中燃烧产生气体R;
③Y的气态氢化物与W的气态氢化物相遇时有白烟生成.
请回答:
(1)X2-的结构示意图为


(2)元素W在元素周期表中的位置是
第二周期ⅤA族
第二周期ⅤA族
.(3)元素Z的单质在空气中燃烧产物的化学式为
Na2O2
Na2O2
.(4)元素Z的最高价氧化物的水化物是一种强碱,写出元素V的单质与该强碱溶
反应的化学方程式
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
:.(5)向Y单质的水溶液中通入过量气体R的现象为
溶液由淡黄绿色逐渐褪至无色
溶液由淡黄绿色逐渐褪至无色
;反应的离子方程式为
Cl2+SO2+2H2O=4H++SO42+2Cl-
Cl2+SO2+2H2O=4H++SO42+2Cl-
.分析:X、Y、Z、V、W五种短周期元素:Y的气态氢化物与W的气态氢化物相遇时有白烟生成,为氨气与HCl反应;X2-、Y-与Y的气态氢化物分子具有相同的电子数,则Y为氯元素、X为硫元素,故W为N元素;X单质在空气中燃烧产生气体R,则R为SO2;Z+、V3+均与W的气态氢化物分子具有相同的电子数,含有10个电子,则Z为Na、V为Al,据此解答.
解答:解:X、Y、Z、V、W五种短周期元素:Y的气态氢化物与W的气态氢化物相遇时有白烟生成,为氨气与HCl反应;X2-、Y-与Y的气态氢化物分子具有相同的电子数,则Y为氯元素、X为硫元素,故W为N元素;X单质在空气中燃烧产生气体R,则R为SO2;Z+、V3+均与W的气态氢化物分子具有相同的电子数,含有10个电子,则Z为Na、V为Al,
(1)X为硫元素,S2-的结构示意图为 ,故答案为:
,故答案为: ;
;
(2)W为N元素,元素周期表中的位置是第二周期ⅤA 族,故答案为:第二周期ⅤA 族;
(3)Z为Na元素,单质在空气中燃烧产物的化学式为Na2O2,故答案为:Na2O2;
(4)铝与氢氧化钠溶液反应生成偏铝酸钠与氢气,反应方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(5)向氯水中通入过量二氧化硫,发生反应:Cl2+SO2+2H2O=4H++SO42+2Cl-,故现象为:溶液由淡黄绿色逐渐褪至无色,
故答案为:溶液由淡黄绿色逐渐褪至无色;Cl2+SO2+2H2O=4H++SO42+2Cl-.
(1)X为硫元素,S2-的结构示意图为
 ,故答案为:
,故答案为: ;
;(2)W为N元素,元素周期表中的位置是第二周期ⅤA 族,故答案为:第二周期ⅤA 族;
(3)Z为Na元素,单质在空气中燃烧产物的化学式为Na2O2,故答案为:Na2O2;
(4)铝与氢氧化钠溶液反应生成偏铝酸钠与氢气,反应方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(5)向氯水中通入过量二氧化硫,发生反应:Cl2+SO2+2H2O=4H++SO42+2Cl-,故现象为:溶液由淡黄绿色逐渐褪至无色,
故答案为:溶液由淡黄绿色逐渐褪至无色;Cl2+SO2+2H2O=4H++SO42+2Cl-.
点评:本题考查结构性质位置关系、常用化学用语、元素化合物性质等,难度中等,推断元素是解题关键,注意对基础知识的理解掌握.

练习册系列答案
相关题目