题目内容
某晶体由两种阳离子、一种阴离子和结晶水组成,取少量该晶体进行如下实验:
①将晶体置于试管中加热,试管口有液体生成;
②待试管冷却后,加水使固体全部溶解;
③向试管中逐滴加入Ba(OH)2溶液至过量,同时加热,沉淀的物质的量先增多后减少,但最终仍有沉淀未溶解,在此过程中还有刺激性气味气体生成.
根据以上实验判断,该晶体是( )
①将晶体置于试管中加热,试管口有液体生成;
②待试管冷却后,加水使固体全部溶解;
③向试管中逐滴加入Ba(OH)2溶液至过量,同时加热,沉淀的物质的量先增多后减少,但最终仍有沉淀未溶解,在此过程中还有刺激性气味气体生成.
根据以上实验判断,该晶体是( )
| A、KAl(SO4)2?12H2O | B、NH4Al(SO4)2?12H2O | C、(NH4)2Fe(SO4)2?6H2O | D、KCl?MgCl2?6H2O |
分析:由③向试管中逐滴加入Ba(OH)2溶液至过量,同时加热,沉淀的物质的量先增多后减少,但最终仍有沉淀未溶解,在此过程中还有刺激性气味气体生成,
则最后的沉淀为硫酸钡、气体为氨气,由沉淀的量的变化可知,有氢氧化铝沉淀生成,以此来解答.
则最后的沉淀为硫酸钡、气体为氨气,由沉淀的量的变化可知,有氢氧化铝沉淀生成,以此来解答.
解答:解:由③向试管中逐滴加入Ba(OH)2溶液至过量,同时加热,沉淀的物质的量先增多后减少,但最终仍有沉淀未溶解,在此过程中还有刺激性气味气体生成,
则最后的沉淀为硫酸钡、气体为氨气,由沉淀的量的变化可知,有氢氧化铝沉淀生成,
由元素守恒可知,该晶体中一定存在硫酸根离子、铝离子、铵根离子,
只有选项B符合,
故选B.
则最后的沉淀为硫酸钡、气体为氨气,由沉淀的量的变化可知,有氢氧化铝沉淀生成,
由元素守恒可知,该晶体中一定存在硫酸根离子、铝离子、铵根离子,
只有选项B符合,
故选B.
点评:本题考查物质的检验,侧重硫酸根离子、铵根离子、铝离子检验的考查,把握③中实验现象与结论的关系为解答的关键,注意沉淀的量的变化,题目难度不大.

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目
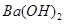 溶液至过量,同时加热,沉淀的物质的量先增多后减少,但最终仍有沉淀未溶解,在此过程中还有刺激性气味气体生成。
溶液至过量,同时加热,沉淀的物质的量先增多后减少,但最终仍有沉淀未溶解,在此过程中还有刺激性气味气体生成。 B.
B.
 D.
D.