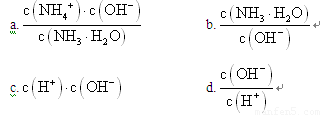��Ŀ����
̼����Ԫ�ؼ��仯�������������������������ء��Իش������й����⣺
��1��NH3��������ˮ����ˮ��Һ�׳ư�ˮ����ˮϡ��0.1mol?L-1�İ�ˮ����Һ������ˮ�������Ӷ���С���� ������ţ���
A��![]() B��
B��![]()
C��c(H+)?c(OH-) D��![]()
��2����״���£���1.12LCO2ͨ��100mL mol?L-1��NaOH��Һ�У�������Һ������Ũ���ɴ�С��˳��Ϊ ��
����Һ������Ũ�ȷ���������е�ʽ��
��c(OH-)=2c(H2CO3)+ ��
��c(H+)+c(Na+)= ��
��3������ȼ�ϵ���з����Ļ�ѧ��ӦΪ��CH4+2O2=CO2+2H2O���õ�صĵ������ҺΪH2SO4��Һ����ԭ��ع���ʱ�������Һ���������ƶ��������� ��
��1��b��d��2�֣����1����1�֣����1����0�֣�
��2��c(Na+)>c(CO2-3)>c(OH-)>c(HCO-3)>c(H+)��2�֣�
��c(H+)+c(HCO-=3)��2�֣�
��2c(CO2-3)+c(HCO-3)+c(OH-)��2�֣�
��3��H+��2�֣�

 ϰ�⾫ѡϵ�д�
ϰ�⾫ѡϵ�д�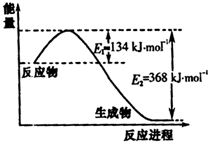
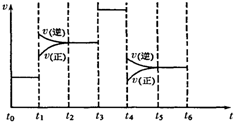
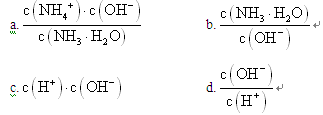
 ԭ��ع���ʱ�������Һ���������ƶ���������_____________��
ԭ��ع���ʱ�������Һ���������ƶ���������_____________��