��Ŀ����
����Ŀ��
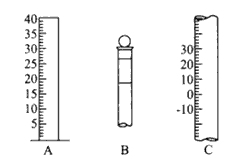
I������ͼ��ʾΪ���������IJ��ֽṹ����д�������������ƣ�A___________��B___________��C____________
II����ͼΪʵ��װ�á�
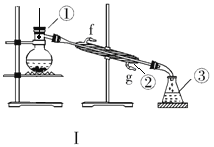
��1��д���������������ƣ���__________��_____________��____________��
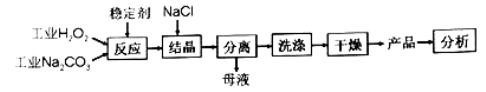
��2��������װ��I�������Ȼ�̼�;ƾ��Ļ�����ȱ�ٵ�������____________________��������������������е�ʵ�����������Ϊ_____________________��
III���������е�����ѧ��ѧʵ�����м��ֳ����IJ���������
���¶ȼ� ������ƿ �������� ���ձ� ��Բ����ƿ ����Ͳ ����Һ©��
��1���������ϱ�������ʹ���¶ȵ���(�������¶ȼ�)_____________ _____(��д���)��������Ӧ�������ɼ��ȵ���__________________(����);ʹ��ʱ�������Ƿ�©ˮ__________________��(�����)
��2��������Ҫ���¶ȼƵ�ʵ����_________________(��д���)��
�������յ��CCl4��Һ�е�CCl4 ��Ũ����ϡ�� ���ⶨ����ص��ܽ��
���𰸡�I����Ͳ������ƿ���¶ȼ�
II����1��������ƿ�������ܣ���ƿ����2���ƾ��ƣ�����
III����1���ڢ����ܢ����ڢ�����2���٢�
�����������������I�����������Ľṹ�����������ֱ�ΪA����Ͳ��B������ƿ��C���¶ȼƣ��ʴ�Ϊ����Ͳ������ƿ���¶ȼƣ�
II����1������װ��ͼ�������Ľṹ������������ƿ�����������ܣ�������ƿ���ʴ�Ϊ��������ƿ�������ܣ���ƿ��
��2����2���������Ȼ�̼�;ƾ��Ļ����������ķ������룬�����þƾ��ƣ��ʴ�Ϊ���ƾ��ƣ�����
III����1���������ϱ�������ʹ���¶ȵ�������ƿ����Ͳ��������Ӧ�������ɼ��ȵ����ձ���Բ����ƿ��ʹ��ʱ�������Ƿ�©ˮ������ƿ����Һ©�����ʴ�Ϊ���ڢ����ܢ����ڢ���
��2���������յ��CCl4��Һ�е�CCl4��Ҫ���¶ȼƿ����¶ȣ���ȷ����Ũ����ϡ�ͣ�����Ҫ�¶ȼƿ����¶ȣ��������ⶨ����ص��ܽ�ȣ���Ҫ���¶ȼƿ����¶ȣ���ȷ����ѡ�٢���

 ��У����ϵ�д�
��У����ϵ�д�