题目内容
配制一定物质的量浓度的NaOH溶液时,造成实验结果偏低的原因是( )
| A.容量瓶中原有少量蒸馏水 | B.称量的NaOH中混有KOH固体 |
| C.定容时俯视观察液面 | D.溶解NaOH后,未冷却就转移到容量瓶 |
B
试题分析:根据
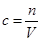 可知,容量瓶中含有蒸馏水不能影响浓度。称量的NaOH中混有KOH固体,说明氢氧化钠的物质的量减少,则浓度偏低。定容时俯视观察液面,则容量瓶中溶液的体积偏少,浓度偏高。溶解NaOH后,未冷却就转移到容量瓶,则根据热胀冷缩可知,冷却后容量瓶中溶液的体积偏少,浓度偏高,答案选B。
可知,容量瓶中含有蒸馏水不能影响浓度。称量的NaOH中混有KOH固体,说明氢氧化钠的物质的量减少,则浓度偏低。定容时俯视观察液面,则容量瓶中溶液的体积偏少,浓度偏高。溶解NaOH后,未冷却就转移到容量瓶,则根据热胀冷缩可知,冷却后容量瓶中溶液的体积偏少,浓度偏高,答案选B。点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重对学生能力的培养和训练,有利于培养学生的逻辑推理能力,提高学生分析问题、解决问题的能力。该类试题需要注意的是根据cB=nB/V可得,一定物质的量浓度溶液配制的误差都是由溶质的物质的量nB和溶液的体积V引起的。误差分析时,关键要看配制过程中引起n和V怎样的变化。在配制一定物质的量浓度溶液时,若nB比理论值小,或V比理论值大时,都会使所配溶液浓度偏小;若nB比理论值大,或V比理论值小时,都会使所配溶液浓度偏大。

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案
相关题目
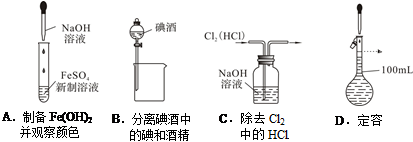
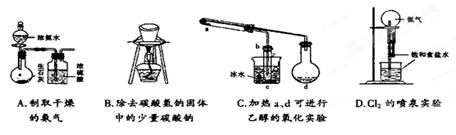
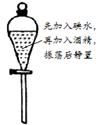
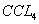 莘取,然后再分液
莘取,然后再分液