题目内容
(2011?海南)铜是重要金属,Cu的化合物在科学研究和工业生产中具有许多用途,如CuSO4溶液常用作电解液、电镀液等.请回答以下问题:
(1)CuSO4可由金属铜与浓硫酸反应制备,该反应的化学方程式为
(2)CuSO4粉末常用来检验一些有机物中的微量水分,其原因是
(3)SO
的立体构型是
(4)元素金(Au)处于周期表中的第六周期,与Cu同族,Au原子最外层电子排布式为
(5)上述晶体具有储氢功能,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中.若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构为CaF2的结构相似,该晶体储氢后的化学式应为
(1)CuSO4可由金属铜与浓硫酸反应制备,该反应的化学方程式为
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
| ||
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
;
| ||
(2)CuSO4粉末常用来检验一些有机物中的微量水分,其原因是
无水是白色,吸水后是蓝色
无水是白色,吸水后是蓝色
;(3)SO
2- 4 |
正四面体结构
正四面体结构
,其中S原子的杂化轨道类型是SP3
SP3
;(4)元素金(Au)处于周期表中的第六周期,与Cu同族,Au原子最外层电子排布式为
6s1
6s1
;一种铜合金晶体具有立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子数量之比为3:1
3:1
;该晶体中,原子之间的作用力是金属键键合力
金属键键合力
;(5)上述晶体具有储氢功能,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中.若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构为CaF2的结构相似,该晶体储氢后的化学式应为
Cu3AuH8
Cu3AuH8
.分析:(1)Cu和浓硫酸在加热条件下反应生成二氧化硫和硫酸铜;
(2)水和硫酸铜粉末形成蓝色CuSO4?5H2O晶体;
(3)根据价层电子对互斥模型判断;
(4)元素金(Au)处于周期表中的第六周期,与Cu同族,则最外层电子数为1,以此判断电子排布式,利用均摊法计算晶胞;
(5)CaF2的结构如图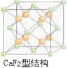 ,利用均摊法计算.
,利用均摊法计算.
(2)水和硫酸铜粉末形成蓝色CuSO4?5H2O晶体;
(3)根据价层电子对互斥模型判断;
(4)元素金(Au)处于周期表中的第六周期,与Cu同族,则最外层电子数为1,以此判断电子排布式,利用均摊法计算晶胞;
(5)CaF2的结构如图
 ,利用均摊法计算.
,利用均摊法计算.解答:解:(1)Cu和浓硫酸在加热条件下反应生成二氧化硫和硫酸铜,
反应的方程式为Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O,
故答案为:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O;
(2)水和硫酸铜粉末形成蓝色CuSO4?5H2O晶体,而硫酸铜粉末为白色,故答案为:无水是白色,吸水后是蓝色;
(3)硫酸根中心原子的价层电子对为:孤对电子数
=0,成键电子对数4,所以为正四面体结构,中心原子为sp3杂化;
故答案为:正四面体结构;SP3;
(4)元素金(Au)处于周期表中的第六周期,与Cu同族,则最外层电子数为1,则最外层电子排布式为6s1,在晶胞中Cu原子处于面心,N(Cu)=6×
=3,Au原子处于顶点位置,N(Au)=8×
=1,则该合金中Cu原子与Au原子数量之比为3:1,为金属晶体,原子间的作用力为金属键键合力,
故答案为:6s1;3:1;金属键键合力;
(5)CaF2的结构如图 ,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中,则H原子应位于晶胞内部,则应含有8个H,则化学式为Cu3AuH8,
,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中,则H原子应位于晶胞内部,则应含有8个H,则化学式为Cu3AuH8,
故答案为:Cu3AuH8.
反应的方程式为Cu+2H2SO4(浓)
| ||
故答案为:Cu+2H2SO4(浓)
| ||
(2)水和硫酸铜粉末形成蓝色CuSO4?5H2O晶体,而硫酸铜粉末为白色,故答案为:无水是白色,吸水后是蓝色;
(3)硫酸根中心原子的价层电子对为:孤对电子数
| 6+2-2×4 |
| 2 |
故答案为:正四面体结构;SP3;
(4)元素金(Au)处于周期表中的第六周期,与Cu同族,则最外层电子数为1,则最外层电子排布式为6s1,在晶胞中Cu原子处于面心,N(Cu)=6×
| 1 |
| 2 |
| 1 |
| 8 |
故答案为:6s1;3:1;金属键键合力;
(5)CaF2的结构如图
 ,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中,则H原子应位于晶胞内部,则应含有8个H,则化学式为Cu3AuH8,
,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中,则H原子应位于晶胞内部,则应含有8个H,则化学式为Cu3AuH8,故答案为:Cu3AuH8.
点评:本题侧重于考查非极性分子的判断、硫酸铜的制备方程式、水的检验方法、杂化轨道理论和立体构型、元素周期律的应用、元素的核外电子排布式等知识,题目难度中等,答题时注意根据信息得出合理推论.

练习册系列答案
相关题目