题目内容
常温下,下列各组物质中,Y既能与X反应又能与Z反应的是
| A.①③ | B.①④ | C.②④ | D.②③ |
B
解析试题分析:第①组Y[Al(OH)3]为两性氢氧化物,既能与强碱又能与强酸反应,正确;第②组SiO2不与盐酸反应,错误;第③组常温下N2既不与O2反应,又不与H2反应,错误;第④组常温下Cu既与FeCl3反应,又与浓硝酸反应,正确。
考点:考查无机化合物间的转化(反应)。

资料:(1)草酸亚铁晶体(FeC2O4·2H2O)呈淡黄色;(2)KMnO4在酸性条件的还原产物为Mn2+。某课题组为探究草酸亚铁晶体的化学性质,进行了一系列实验探究。
(1)向盛有草酸亚铁晶体的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现溶液颜色逐渐变为棕黄色,并检测到CO2生成。这说明草酸亚铁晶体具有 (填“氧化性”、“还原性”或“碱性”)。若反应中消耗1 mol FeC2O4·2H2O,则参加反应的KMnO4为 ______mol。
(2)资料表明:在密闭容器中加热到一定温度时,草酸亚铁晶体可完全分解,生成几种氧化物,残留物为黑色固体。课题组根据课本上所介绍的铁的氧化物的性质,对黑色固体的组成提出如下假设,请你完成假设二和假设三:
假设一:全部是FeO;假设二: ;假设三:
(3)为验证上述假设一是否成立,课题组进行如下研究。
【定性研究】请你完成下表中内容。
| 实验步骤(不要求具体的操作过程) | 预期实验现象和结论 |
| 取少量黑色固体, | |
【定量研究】课题组在文献中查阅到,FeC2O4·2H2O受热分解时,固体质量随温度变化的曲线如下图所示,写出加热到400℃时,FeC2O4·2H2O晶体受热分解的化学方程式为: 。
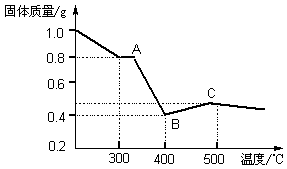
根据图象,如有1.0 g草酸亚铁晶体在坩埚中敞口充分加热,最终残留黑色固体的质量大于0.4 g。某同学由此得出结论:假设一不成立。你是否同意该同学的结论 (填“同意”或“不同意”),并简述理由 。
Fe(OH)3胶体虽然是由FeCl3溶液制得,但两者是截然不同的两种物质。FeCl3溶液、Fe(OH)3胶体共同具备的性质是 ( )
| A.都呈透明的红褐色 |
| B.都比较稳定,密封保存一段时间都不会产生沉淀 |
| C.分散质颗粒直径相同 |
| D.当有光线透过时,都能产生丁达尔效应 |
下列各组物质的分类正确的是
①混合物:氯水、氨水、水银、福尔马林
②电解质:明矾、冰醋酸、石膏、纯碱
③能导电的物质:铜、盐酸、氯化钠晶体
④同位素:1H+、2H2、3H
⑤同素异形体:C60、C80、金刚石、石墨
⑥强电解质:烧碱、碳酸钙、氢氧化钡、氯水
| A.②⑤ | B.②③④⑤ | C.②③⑤⑥ | D.全部正确 |
下列说法正确的是
| A.向饱和硼酸溶液中滴加Na2CO3溶液,有CO2气体生成 |
| B.KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质 |
| C.AgCl沉淀易转化为AgI沉淀且Ksp(AgX)=c(Ag+)·c(X-),故Ksp(AgI)<Ksp(AgCl) |
| D.沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强 |
下列物质中含有共价键的离子化合物是
| A.H2 | B.Na2O2 | C.NaOH | D.H2S |
下列说法正确的是
| A.所谓低碳经济,是指在可持续发展理念指导下,尽可能地减少光化学污染气体的排放 |
| B.汽油、柴油和植物油都是碳氢化合物 |
| C.只由一种元素组成的物质,一定是纯净物 |
| D.化学反应的实质就是旧化学键的断裂、新化学键形成过程 |
辨析以下的说法①l6O与 l8O的转化可以通过化学反应实现;②灼烧钠的化合物时火焰呈黄色,那是发生了化学反应;③碱性氧化物一定是金属氧化物;④只由一种元素组成的物质一定是纯净物;⑤石墨与金刚石的转化是化学变化;⑥糖类、蛋白质、油脂均属于天然高分子化合物;上述说法中正确的是
| A.①④⑤ |
| B.①②④ |
| C.③⑤ |
| D.①③⑥ |
已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去)。则W、X不可能是( )。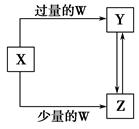
| 选项 | A | B | C | D |
| X | C | Fe | Ca(O H)2溶液 | AlC3 |
| W | O2 | HN3 | CO2 | NH3·H2O |