题目内容
19.有甲、乙、丙、丁四种无色溶液,它们分别是HCl、H2SO4、BaCl2、Na2CO3溶液中的一种.为区别这四种溶液,现将它们两两混合并得到下面现象:| 溶液 | 甲+乙 | 乙+丙 | 丙+丁 | 甲+丁 |
| 现象 | 无明显现象 | 白色沉淀 | 白色沉淀 | 无色气体 |
| A. | HCl、BaCl2、H2SO4、Na2CO3 | B. | H2SO4、HCl、BaCl2、Na2CO3 | ||
| C. | HCl、H2SO4、BaCl2、Na2CO3 | D. | H2SO4、Na2CO3、HCl、BaCl2 |
分析 BaCl2与H2SO4、Na2CO3均反应生成白色沉淀,Na2CO3与HCl、H2SO4反应均生成气体,由表格中的现象可知丙为BaCl2,以此来解答.
解答 解:BaCl2与H2SO4、Na2CO3均反应生成白色沉淀,Na2CO3与HCl、H2SO4反应均生成气体,由表格中乙+丙、丙+丁的现象可知丙为BaCl2,由丙+丁、甲+丁的现象可知,丁为Na2CO3,则乙为H2SO4,从而可知甲为HCl,
故选C.
点评 本题考查无机物的推断,为高频考点,把握物质之间的反应及现象为解答的关键,侧重分析与推断能力的考查,注意元素化合物知识的综合应用,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
10.有关晶体的结构如图所示,下列说法中不正确的是( )


| A. | 在NaCl晶体中,距Na+最近的Cl-形成正八面体 | |
| B. | 在CaF2晶体中,Ca2+、F-的配位数分别是4、8 | |
| C. | 在金刚石晶体中,碳原子与碳碳键个数的比为1:2 | |
| D. | 该气态团簇分子的分子式为EF或FE |
7.如表实验中,所采取的分离方法与对应原理都正确的是( )
| 选项 | 目的 | 分离方法 | 原理 |
| A | 除去Fe(OH)3胶体中的FeCl3 | 过滤 | 分散质微粒的大小不同 |
| B | 除去纯碱中的碳酸氢铵 | 加热 | 稳定性不同 |
| C | 分离KNO3和NaCl | 重结晶 | KNO3的溶解度大于NaCl |
| D | 分离食用油和汽油 | 分液 | 食用油和汽油的密度不同 |
| A. | A | B. | B | C. | C | D. | D |
11.NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | lmol FeI2与足量氯气反应时转移的电子数为2NA | |
| B. | 乙烯和丙烯组成的42 g混合气体中氢原子的个数为6 NA | |
| C. | 1 mol Na2O2固体中含离子总数为4NA | |
| D. | 2 L0.5 mol•L-1硫酸钾溶液中阴离子所带电荷数为NA |
8.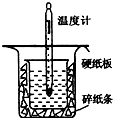 中和热的测定是高中重要的定量实验.取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于图所示的装置中进行中和热的测定实验,回答下列问题:
中和热的测定是高中重要的定量实验.取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于图所示的装置中进行中和热的测定实验,回答下列问题:
(1)从如图实验装置看,其中尚缺少的一种玻璃用品是环形玻璃搅拌棒,除此之外,装置中的一个明显错误是大烧杯杯口与小烧杯杯口没有相平.
(2)为保证该实验成功该同学采取了许多措施,如图的碎纸条的作用在于隔热,减少热量的损失.
(3)若改用60mL 0.25mol•L-1H2SO4和50mL 0.55mol•L-1NaOH溶液进行反应与上述实验相比,所放出的热量不相等(填“相等”、“不相等”),若实验操作均正确,则所求中和热相等填“相等”“不相等”)
(4)倒入NaOH溶液的正确操作是:C. (从下列选出).
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
(5)使硫酸与NaOH溶液混合均匀的正确操作是:D. (从下列选出).
A.用温度计小心搅拌
B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯
D.用套在温度计上的环形玻璃棒轻轻地搅动
(6)实验数据如下表:
①请填写下表中的空白:
②近似认为0.55mol/L NaOH溶液和0.25mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g•℃).则中和热△H=-56.8kJ/mol( 取小数点后一位).
③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)abc.
a.实验装置保温、隔热效果差
b.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中.
 中和热的测定是高中重要的定量实验.取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于图所示的装置中进行中和热的测定实验,回答下列问题:
中和热的测定是高中重要的定量实验.取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于图所示的装置中进行中和热的测定实验,回答下列问题:(1)从如图实验装置看,其中尚缺少的一种玻璃用品是环形玻璃搅拌棒,除此之外,装置中的一个明显错误是大烧杯杯口与小烧杯杯口没有相平.
(2)为保证该实验成功该同学采取了许多措施,如图的碎纸条的作用在于隔热,减少热量的损失.
(3)若改用60mL 0.25mol•L-1H2SO4和50mL 0.55mol•L-1NaOH溶液进行反应与上述实验相比,所放出的热量不相等(填“相等”、“不相等”),若实验操作均正确,则所求中和热相等填“相等”“不相等”)
(4)倒入NaOH溶液的正确操作是:C. (从下列选出).
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
(5)使硫酸与NaOH溶液混合均匀的正确操作是:D. (从下列选出).
A.用温度计小心搅拌
B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯
D.用套在温度计上的环形玻璃棒轻轻地搅动
(6)实验数据如下表:
①请填写下表中的空白:
| 温度 实验次数 | 起始温度t1℃ | 终止温度t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 29.5 | 3.4 |
| 2 | 27.0 | 27.4 | 27.2 | 32.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 | |
| 4 | 26.4 | 26.2 | 26.3 | 29.8 | |
③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)abc.
a.实验装置保温、隔热效果差
b.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中.