题目内容
铜和镁的合金4.6g完全溶于浓硝酸,若反应中硝酸被还原只生4480mL的 气体和336mL的
气体和336mL的 气体(都已折算到标准状况),在应后的溶液中,加入足量的氢氧化钠溶液,生成沉淀的质量是
气体(都已折算到标准状况),在应后的溶液中,加入足量的氢氧化钠溶液,生成沉淀的质量是
[ ]
A.9.02g
B.8.51g
C.8.26g
D.7.04g
答案:B
解析:
解析:
|
因相当于放出  气体共0.23mol,根据得失电子守恒可知,Cu和Mg的物质的量之和为0.115mol,即生成氢氧化物 气体共0.23mol,根据得失电子守恒可知,Cu和Mg的物质的量之和为0.115mol,即生成氢氧化物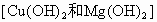 的物质量之和为0.115mol,其增重的 的物质量之和为0.115mol,其增重的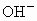 的物质的量为2×0.115mol,其质量为2×0.115mol×l7/mol=3.91g,则所得氢氧化物的质量为4.6g+3.91g=8.51g. 的物质的量为2×0.115mol,其质量为2×0.115mol×l7/mol=3.91g,则所得氢氧化物的质量为4.6g+3.91g=8.51g. |

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
铜和镁的合金4.6g完全溶于浓硝酸,若反应中硝酸被还原只产生4480mL的NO2气体和336mlN2O4(都已折算到标准状况),在反应后的溶液中,加入足量的氢氧化钠溶液,生成沉淀的质量为( )。
| A.8.51g | B.8.26g | C.7.04g | D.9.02g |