题目内容
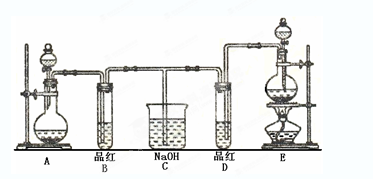
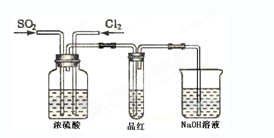
(10分)下图为实验室制取纯净、干燥的Cl2,并进行检验Cl2性质实验的装置。其中D瓶中放有干燥红色布条;E中为铜网,E右端出气管口附近为石棉球。
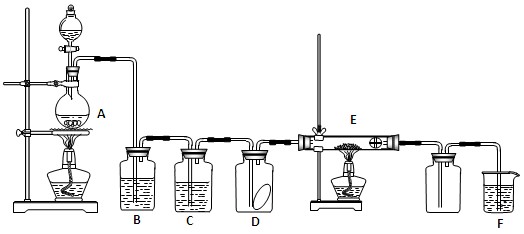
试回答:
(1)A中发生反应的方程式为_____________ _________________________________;
(2)为得到干燥纯净的氯气,一般在B瓶中加入饱和食盐水,其作用是______________;
(3)C中盛放的试剂为_____________;
(4)E中所发生反应的方程式为____________________________________________。
(5) F中应加入的试剂为 ,其作用是 。
(6)若A中有14.6g HCl 被氧化,将产生的氯气通入足量的KI溶液中能产生单质碘的质量 为_____________g。

试回答:
(1)A中发生反应的方程式为_____________ _________________________________;
(2)为得到干燥纯净的氯气,一般在B瓶中加入饱和食盐水,其作用是______________;
(3)C中盛放的试剂为_____________;
(4)E中所发生反应的方程式为____________________________________________。
(5) F中应加入的试剂为 ,其作用是 。
(6)若A中有14.6g HCl 被氧化,将产生的氯气通入足量的KI溶液中能产生单质碘的质量 为_____________g。
MnO2 +4HCl(浓)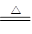 MnCl2 + Cl2↑ + 2H2O ;吸收HCl气体;浓H2SO4;
MnCl2 + Cl2↑ + 2H2O ;吸收HCl气体;浓H2SO4;
Cu + Cl2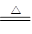 CuCl2 ;碱液;吸收多余的氯气;50.8 g
CuCl2 ;碱液;吸收多余的氯气;50.8 g
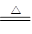 MnCl2 + Cl2↑ + 2H2O ;吸收HCl气体;浓H2SO4;
MnCl2 + Cl2↑ + 2H2O ;吸收HCl气体;浓H2SO4;Cu + Cl2
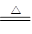 CuCl2 ;碱液;吸收多余的氯气;50.8 g
CuCl2 ;碱液;吸收多余的氯气;50.8 g (1)A是制取氯气的,方程式为MnO2 +4HCl(浓)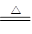 MnCl2 + Cl2↑ + 2H2O。
MnCl2 + Cl2↑ + 2H2O。
(2)由于浓盐酸易挥发,所以生成的氯气中混有氯化氢气体,而氯化氢极易溶于水,所以可以通过饱和食盐水来除去氯气中的氯化氢气体。
(3)D中是干燥的布条,所以要验证其漂白性,氯气应该是干燥的,所以C中是浓硫酸,用来干燥氯气。
(4)氯气具有强氧化性,在加热的条件下,能和铜反应生成氯化铜,方程式为Cu + Cl2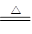 CuCl2 。
CuCl2 。
(5)氯气有毒,属于大气污染物,因此需要尾气处理。可用氢氧化钠等碱液来吸收。
(6)14.6g HCl 被氧化,则生成氯气是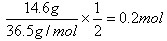 ,因此可用产生0.2mol单质碘,其质量是0.2mol×254g/mol=50.8g。
,因此可用产生0.2mol单质碘,其质量是0.2mol×254g/mol=50.8g。
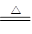 MnCl2 + Cl2↑ + 2H2O。
MnCl2 + Cl2↑ + 2H2O。(2)由于浓盐酸易挥发,所以生成的氯气中混有氯化氢气体,而氯化氢极易溶于水,所以可以通过饱和食盐水来除去氯气中的氯化氢气体。
(3)D中是干燥的布条,所以要验证其漂白性,氯气应该是干燥的,所以C中是浓硫酸,用来干燥氯气。
(4)氯气具有强氧化性,在加热的条件下,能和铜反应生成氯化铜,方程式为Cu + Cl2
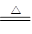 CuCl2 。
CuCl2 。(5)氯气有毒,属于大气污染物,因此需要尾气处理。可用氢氧化钠等碱液来吸收。
(6)14.6g HCl 被氧化,则生成氯气是
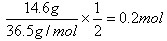 ,因此可用产生0.2mol单质碘,其质量是0.2mol×254g/mol=50.8g。
,因此可用产生0.2mol单质碘,其质量是0.2mol×254g/mol=50.8g。
练习册系列答案
相关题目
 I2+I-,向盛有KI3溶液的试管中加人适量CCl4,振荡静置后CCl4层显紫红色,说明KI3在CCl4中的溶解度比在水中的大
I2+I-,向盛有KI3溶液的试管中加人适量CCl4,振荡静置后CCl4层显紫红色,说明KI3在CCl4中的溶解度比在水中的大