题目内容
【题目】下列关于电解质溶液的叙述正确的是
A. 常温下电离常数为Ka的酸HA溶液中c(H+)![]() mol·L-1
mol·L-1
B. 向0.1 mol·L-1的氨水中加入少量硫酸铵固体,则溶液中c(OH-)/c(NH3·H2O)增大
C. 0.2 mol·L-1CH3COOH溶液与0.1 mol·L-1NaOH溶液等体积混合
2c(H+)-2 c(OH-)=c(CH3COO-)- c(CH3COOH)
D. 将饱和Na2SO4溶液加入到饱和石灰水中,有白色沉淀产生,说明Ksp[Ca(OH)2]大于Ksp(CaSO4)
【答案】C
【解析】A、HA的浓度未知,不能计算氢离子浓度,A错误;B、向0.1 mol·L-1的氨水中加入少量硫酸铵固体,铵根浓度增大,抑制一水合氨的电离,氢氧根浓度减小,氨水浓度增大,则溶液中c(OH-)/c(NH3·H2O)减小,B错误;C、0.2 mol·L-1CH3COOH溶液与0.1 mol·L-1NaOH溶液等体积混合所得溶液是醋酸和醋酸钠等浓度的混合溶液,根据电荷守恒c(H+)+c(Na+)=c(OH-)+c(CH3COO-)和物料守恒2c(Na+)=c(CH3COO-)+c(CH3COO-)可知溶液中
2c(H+)-2 c(OH-)=c(CH3COO-)- c(CH3COOH),C正确;D、只要溶液中浓度熵大于溶度积常数,即可产生沉淀,与溶度积常数相对大小并无直接关系,D错误,答案选C。

【题目】原电池是化学对人类的一项重大贡献。
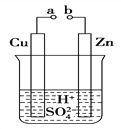
(1)某兴趣小组为研究原电池原理,设计如图A装置。
|
|
A | B |
①a和b不连接时,烧杯中发生反应的离子方程式是 _________________________。
②a和b用导线连接,Cu极为原电池________极(填“正”或“负”),该电极反应式是____________________。
③无论a和b是否连接,Zn片均被腐蚀,若转移了0.2 mol电子, 则理论上Zn片质量减轻________g。
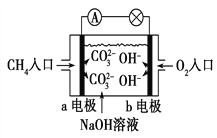
(2)如图是甲烷燃料电池原理示意图B,回答下列问题:
①电池的负极是________(填“a”或“b”)电极,该极的电极反应式为: _________________________。
②电池工作一段时间后电解质溶液的pH__________(填“增大”“减小”或“不变”)。