题目内容
【题目】能源的开发利用与人类社会的可持续性发展息息相关.
(1)①Fe2O3(s)+3C(s)=2Fe(s)+3CO(g)△H1=a kJmol﹣1
②CO(g)+ ![]() O2(g)=CO2(g)△H2=b kJmol﹣1
O2(g)=CO2(g)△H2=b kJmol﹣1
③4Fe(s)+3O2(g)=2Fe2O3(s)△H3=ckJmol﹣1
则C的燃烧热kJmol﹣1
依据原电池的构成原理,下列化学反应在理论上可以设计成原电池的是(填序号).
A.C(s)+CO2(g)═2CO(g)
B.NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)
C.2H2O(l)═2H2(g)+O2(g)
D.2CO(g)+O2(g)═2CO2(g)
若以熔融的K2C03与C02为反应的环境,依据所选反应设计成一个原电池,请写出该原电池的负极反应: .
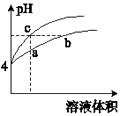
(2)某实验小组模拟工业合成氨反应N2+3H2 ![]() 2NH3 △H=92.4 kJmol﹣1 , 开始他们将N2和H2混合气体20mol(体积比1:1)充入5L合成塔中.反应前压强为P.,反应过程中压强用P表示,反应过程中P/P.与时间t的关系如图2所示.请回答下列问题:
2NH3 △H=92.4 kJmol﹣1 , 开始他们将N2和H2混合气体20mol(体积比1:1)充入5L合成塔中.反应前压强为P.,反应过程中压强用P表示,反应过程中P/P.与时间t的关系如图2所示.请回答下列问题: 
①反应达平衡的标志是(填字母代号) .
A.压强保持不变
B.气体密度保持不变
C.NH3的生成速率是N2的生成速率的2倍
②2min时,以C(N2)变化表示的平均反应速率为 .
③若提高N2的转化率可采取的措施有 .
A.向体系中按体积比1:1再充入N2和H2
B.分离出NH3
C.升高温度
D.充入He气使压强增大
E.加入一定量的N2 .
【答案】
(1)![]() ;D;CO﹣2e﹣+CO32﹣=2CO2
;D;CO﹣2e﹣+CO32﹣=2CO2
(2)AC;0.1mol?L﹣1?min﹣1;AB
【解析】解:(1)①Fe2O3(s)+3C(s)=2Fe(s)+3CO(g)△H1=akJmol﹣1②CO(g)+ ![]() O(g)=CO2(g)△H=bKJ/mol
O(g)=CO2(g)△H=bKJ/mol
③4Fe(s)+3O2(g)=2Fe2O3(s)△H3=ckJmol﹣1
依据盖斯定律①×2+②×6+③,6C(s)+6O2(g)=6CO2(g)△H=(2a+6b+c)kJmol﹣1
碳的燃烧热C(s)+O2(g)=CO2(g)△H= ![]() kJmol﹣1
kJmol﹣1
所以答案是: ![]() ;
;
电池的构成原理是自发进行的氧化还原化学反应在理论上可以设计成原电池
A.C(s)+CO2(g)═2CO(g),是吸热反应,不能涉及成原电池,故A不符合;
B.NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)是复分解反应,不是氧化还原反应,故B不符合;
C.2H2O(l)═2H2(g)+O2(g)反应是非自发进行的氧化还原反应,故C不符合;
D.2CO(g)+O2(g)═2CO2(g),反应是自发进行的氧化还原反应,故D符合;
一氧化碳燃料电池在熔融的K2CO3与CO2为反应的环境中,传到离子为碳酸根离子,负极是一氧化碳失电子生成二氧化碳,电极反应为:CO﹣2e﹣+CO32﹣=2CO2 ;
所以答案是:D;CO﹣2e﹣+CO32﹣=2CO2 ;(2)①氮气和氢气合成氨气的反应是气体体积减小的放热反应,反应达到平衡的标志是正逆反应速率相同,各组分含量保持不变;
A.反应是气体体积变化的反应,压强保持不变说明反应达到平衡,故A正确;
B.反应过程中气体质量不变,体积不变,反应过程中密度不变,气体密度保持不变,不能说明反应达到平衡,故B错误;
C.NH3的生成速率是N2的生成速率的2倍,说明正逆反应反应速率相同,反应达到平衡,故C正确;
所以答案是:AC; ②2min时压强之比为P;Po=0.9,相同条件下气体物质的量之比等于压强之比,设反应后的气体物质的量为n,则P:Po=n:20=0.9,n=18mol,反应前后物质的量减小2mol,依据反应的过程分析,减少的物质的量为生成的氨气物质的量,氨气表示的反应速率= ![]() =0.2mol/Lmin,依据反应速率之比等于化学方程式系数之比得到氮气表示的反应速率为0.11molL﹣1min﹣1;
=0.2mol/Lmin,依据反应速率之比等于化学方程式系数之比得到氮气表示的反应速率为0.11molL﹣1min﹣1;
所以答案是:0.1molL﹣1min﹣1;③提高N2的转化率可采取的措施是平衡正向进行
A.向体系中按体积比1:1再充入N2和H2,恒温恒容容器中计入铜比例的起始量相当于增大压强,平衡正向进行,氮气的转化率增大,故A符合;
B.分离出NH3 , 平衡正向进行,氮气的转化率增大,故B符合;
C.反应是吸热反应,升高温度平衡逆向进行,氮气的转化率减小,故C不符合;
D.充入He气使压强增大,恒温恒容容器中 气体分压不变,平衡不动,故D不符合;
E.加入一定量的N2,提高氢气的转化率,打不起的转化率减小,故E不符合;
所以答案是:AB.
【考点精析】关于本题考查的化学平衡状态本质及特征和化学平衡状态的判断,需要了解化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效);状态判断:①v(B耗)=v(B生)②v(C耗):v(D生)=x : y③c(C)、C%、n(C)%等不变④若A、B、C、D为气体,且m+n≠x+y,压强恒定⑤体系颜色不变⑥单位时间内某物质内化学键的断裂量等于形成量⑦体系平均式量恒定(m+n ≠ x+y)等才能得出正确答案.

【题目】实验室用密度为1.25gmL﹣1、质量分数为36.5%的浓盐酸配制240mL 0.1molL﹣1的盐酸,请回答下列问题:
(1)浓盐酸的物质的量浓度为 .
(2)配制 240mL 0.1molL﹣1 的盐酸
应量取浓盐酸体积/mL | 应选用容量瓶的规格/mL |
(3)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次 ) .
A.用30mL水洗涤烧杯内壁和玻璃棒23次,洗涤液均注入容量瓶,振荡
B.用量筒淮确量取所需的浓盐酸的体积,倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线12cm处
(4)若实验中遇到下列情况,对盐酸溶液的物质的量浓度有何影响(填“偏高”、“偏低”或“不变”)?
①用于稀释盐酸的烧杯未洗涤, .
②容量瓶中原有少量蒸馏水, .
③定容时观察液面俯视, .
(5)若实验过程中出现如下情况如何处理?
①定容时加蒸馏水时超过了刻度 .
②向容量瓶中转移溶液时有滚液不慎有溶液溅出 .
③定容摇勻后发现液面下降 .