题目内容
设NA为阿佛加德罗常数,下列叙述中正确的是
- A.常温常压下,11.2L氧气所含的原子数为NA
- B.常温常压下,48gO3含有的氧原子数3NA
- C.1.8g的NH4+中含有的电子数为10NA
- D.2.4g金属镁变为镁离子时失去的电子数为0.1NA
B
分析:A、气体摩尔体积vm=22.4L/mol使用条件是标准状况(0°C,101kPa);
B、根据n= 计算n(O),利用N(O)=n(O)?NA求算判断;
计算n(O),利用N(O)=n(O)?NA求算判断;
C、先求出NH4+数目,电子的数目是NH4+数目的10倍,
D、先求出镁原子数目,由于一个镁原子失去2e-变为镁离子,失去电子数是镁原子数目2倍.
解答:A、不是标准状况,不能使用气体摩尔体积vm=22.4L/mol,11.2L氧气的物质的量不是0.5mol,所含的原子数不是NA,故A错误;
B、n(O)=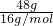 =3mol,48gO3含有的氧原子数为N(O)=n(O)?NA=3mol×NAmol-1=3NA,故B正确;
=3mol,48gO3含有的氧原子数为N(O)=n(O)?NA=3mol×NAmol-1=3NA,故B正确;
C、1.8g的NH4+含有的NH4+数目为N(NH4+)=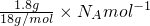 =0.1NA,电子的数目为10×0.1NA=NA,故C错误;
=0.1NA,电子的数目为10×0.1NA=NA,故C错误;
D、2.4g金属镁含有镁原子数目N(Mg)=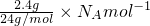 =0.1NA,失去电子数为2×0.1NA=0.2NA,故D错误.
=0.1NA,失去电子数为2×0.1NA=0.2NA,故D错误.
故选B.
点评:解答阿伏伽德罗常数问题注意:特殊物质的摩尔质量、某些物质分子中的原子个数、一些物质中的化学键、较复杂的化学反应中电子数的求算、某些离子或原子团在水溶液中能发生水解、气体摩尔体积vm=22.4L/mol的使用条件及范围等.
分析:A、气体摩尔体积vm=22.4L/mol使用条件是标准状况(0°C,101kPa);
B、根据n=
 计算n(O),利用N(O)=n(O)?NA求算判断;
计算n(O),利用N(O)=n(O)?NA求算判断;C、先求出NH4+数目,电子的数目是NH4+数目的10倍,
D、先求出镁原子数目,由于一个镁原子失去2e-变为镁离子,失去电子数是镁原子数目2倍.
解答:A、不是标准状况,不能使用气体摩尔体积vm=22.4L/mol,11.2L氧气的物质的量不是0.5mol,所含的原子数不是NA,故A错误;
B、n(O)=
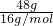 =3mol,48gO3含有的氧原子数为N(O)=n(O)?NA=3mol×NAmol-1=3NA,故B正确;
=3mol,48gO3含有的氧原子数为N(O)=n(O)?NA=3mol×NAmol-1=3NA,故B正确;C、1.8g的NH4+含有的NH4+数目为N(NH4+)=
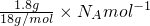 =0.1NA,电子的数目为10×0.1NA=NA,故C错误;
=0.1NA,电子的数目为10×0.1NA=NA,故C错误;D、2.4g金属镁含有镁原子数目N(Mg)=
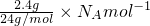 =0.1NA,失去电子数为2×0.1NA=0.2NA,故D错误.
=0.1NA,失去电子数为2×0.1NA=0.2NA,故D错误.故选B.
点评:解答阿伏伽德罗常数问题注意:特殊物质的摩尔质量、某些物质分子中的原子个数、一些物质中的化学键、较复杂的化学反应中电子数的求算、某些离子或原子团在水溶液中能发生水解、气体摩尔体积vm=22.4L/mol的使用条件及范围等.

练习册系列答案
相关题目
设NA、表示阿佛加德罗常数值,下列说法正确的是
| A.1000mL0.1mol·L-1的Al2(SO4)3溶液中,含Al3+ 0.1NA |
| B.在标准状况下,11.2L氖气中含有NA个氖原子 |
| C.7.8gNa2O2与足量CO2反应,转移电子数为0.1NA |
| D.62 g Na2O溶于水后所得溶液中含有O2-离子数为NA |