题目内容
在一固定容积的密闭容器中进行如下反应:2SO (g)+O
(g)+O (g)
(g) 2SO
2SO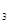 (g),已知反应进行到10秒时,SO
(g),已知反应进行到10秒时,SO 、O
、O 、SO
、SO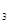 的物质的量分别为0.2 mol、0.1 mol、0.2 mol,则下列说法正确的是
的物质的量分别为0.2 mol、0.1 mol、0.2 mol,则下列说法正确的是
 (g)+O
(g)+O (g)
(g) 2SO
2SO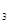 (g),已知反应进行到10秒时,SO
(g),已知反应进行到10秒时,SO 、O
、O 、SO
、SO 的物质的量分别为0.2 mol、0.1 mol、0.2 mol,则下列说法正确的是
的物质的量分别为0.2 mol、0.1 mol、0.2 mol,则下列说法正确的是A.10秒时,用O 表示该反应的平均反应速率为0.01 mol/(L·s) 表示该反应的平均反应速率为0.01 mol/(L·s) |
B.当反应达平衡时,SO 的物质的量可能为0.4 mol 的物质的量可能为0.4 mol |
C.当SO 和O 和O 的生成速率之比为2:1时,达到该反应限度 的生成速率之比为2:1时,达到该反应限度 |
D.向容器内充人SO ,可以提高反应速率 ,可以提高反应速率 |
D
试题分析:反应进行到10s时生成三氧化硫0.2mol,则消耗氧气是0.1mol。由于不能确定容器的体积,所以不能计算该反应的反应速率是,A不正确;根据S原子守恒可知,SO2和SO3的物质的量之和是0.4mol,由于反应是可逆反应,反应物的转化率达不到100%,所以当反应达平衡时,SO3的物质的量不可能为0.4 mol,B不正确;反应速率之比是相应的化学计量数之比,所以二氧化硫和氧气的反应速率总是2:1的,C不正确;向容器内充人SO2,增大SO2的浓度,可以提高反应速率,D正确,答案选D。
点评:该题是中等难度的试题,也是高考中的常见题型。试题针对性强,贴近高考,注重答题的灵活性,有利于培养学生的逻辑推理能力和抽象思维能力。易错点是选项A。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 zC(g) ΔH>0,平衡时测得A的浓度为0.50mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时, 测得A的浓度为0.30mol/L。下列有关判断正确的是
zC(g) ΔH>0,平衡时测得A的浓度为0.50mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时, 测得A的浓度为0.30mol/L。下列有关判断正确的是 Si3N4(s) + 6CO(g) + Q(Q>0)
Si3N4(s) + 6CO(g) + Q(Q>0)
 CH3OCH3(g) +H2O(g) △H,其CO的平衡转化率随温度、压强变化关系如图所示,下列说法正确的是
CH3OCH3(g) +H2O(g) △H,其CO的平衡转化率随温度、压强变化关系如图所示,下列说法正确的是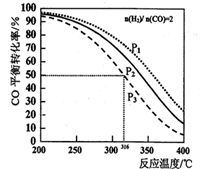
 H2(g) +CO2(g)平衡常数K随温度的变化如下表:
H2(g) +CO2(g)平衡常数K随温度的变化如下表:
 2C0 Cg)平衡常数K1;
2C0 Cg)平衡常数K1; CO Cg) +H2(g)平衡常数K2
CO Cg) +H2(g)平衡常数K2

 2NH3(g) △H<0。在一体积为2L的密闭容积中,加入0.20mol的N2和0.60mol的H2,反应中NH3的物质的量浓度的变化情况如图所示,
2NH3(g) △H<0。在一体积为2L的密闭容积中,加入0.20mol的N2和0.60mol的H2,反应中NH3的物质的量浓度的变化情况如图所示,
 Z(g)达到平衡,正反应速率随时间的变化如图所示,下列叙述不正确的是( )
Z(g)达到平衡,正反应速率随时间的变化如图所示,下列叙述不正确的是( )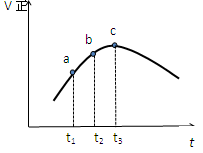
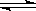 2Fe(s)+3CO2(g)ΔH>0
2Fe(s)+3CO2(g)ΔH>0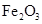 粉末的密闭容器中通入CO气体,10min后,生成了单质铁11.2g。则10min内CO的平均反应速率为
粉末的密闭容器中通入CO气体,10min后,生成了单质铁11.2g。则10min内CO的平均反应速率为