题目内容
甲、乙、丙、丁为前三周期元素形成的粒子,它们的电子总数相等。已知甲、乙、丙为双原子分子或负二价双原子阴离子,丁为原子。(1)丙与钙离子组成的离子化合物跟水反应产生一种可燃性气体,反应的化学方程式是__________。
(2)乙在高温时是一种还原剂,请用化学方程式表示它在工业上的一种重要用途:__________。
(3)在一定条件下,甲与O2反应的化学方程式是__________。
(4)丁的元素符号是__________,它的原子结构示意图为__________。
(5)丁的氧化物的晶体结构与__________的晶体结构相似。
(1)CaC2+2H2O→C2H2↑+Ca(OH)2
(2)例如:3CO+Fe2O3![]() 2Fe+3CO2,工业上利用该反应炼铁(其他合理答案也可以)
2Fe+3CO2,工业上利用该反应炼铁(其他合理答案也可以)
(3)N2+O2![]() 2NO
2NO
![]()
(5)金刚石
解析:首先,丙与Ca2+形成的离子化合物与水反应产生一种可燃性气体,可确定丙为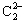 ,该化合物为CaC2,反应的化学方程式为:CaC2+2H2O→Ca(OH)2+C2H2↑。
,该化合物为CaC2,反应的化学方程式为:CaC2+2H2O→Ca(OH)2+C2H2↑。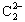 含有电子:6×2+2=14个。即丁为含14个电子的原子,也就是Si原子。甲、乙都是含14个原子的双原子分子,可能为CO或者N2,根据乙在高温下为还原剂,可知甲为N2、乙为CO。
含有电子:6×2+2=14个。即丁为含14个电子的原子,也就是Si原子。甲、乙都是含14个原子的双原子分子,可能为CO或者N2,根据乙在高温下为还原剂,可知甲为N2、乙为CO。

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案
相关题目
