题目内容
【物质结构与性质】
X、Y、Z、W是原子序数依次增大的前四周期元素,已知:
①X元素原子的最外层电子数是次外层的2倍;
②Y元素原子的p轨道上有2个未成对电子;
③Z元素在同一短周期元素中的原子半径最大;
④W元素原子的最外层电子数与Z相同,其余各电子层均充满电子。
请回答下列问题:
(1)X、Y、Z三种元素的第一电离能从小到大的顺序是 (用元素符号表示,下同);
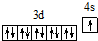
(2)W元素原子核外电子排布式是 ;
(3)Z元素与氢元素形成的化合物熔点比Y元素的氢化物熔点高,原因是 ;
(4)X的一种氢化物相对分子质量为42,分子中含有σ键和π键的个数比为8︰1,则该分子中X原子的杂化类型是 和 。
(5)Y的最简单氢化物可以和W2+形成配位键,而X的最简单氢化物则不行,其原因是 。
(1)Na<C<O (2分)
(2)1s22s22p63s23p63d104s1 (2分)
(3)NaH是离子晶体,熔化时破坏离子键,H2O是分子晶体,熔化时破坏分子间作用力,破坏离子键比破坏分子间作用力所需的能量大 (2分)
(4)sp2、 sp3 (各1分,共2分)
(5)H2O中的O原子中存在孤电子对,而CH4中的C原子没有孤电子对 (2分)
解析:略

 阅读快车系列答案
阅读快车系列答案 或
或