题目内容
 某兴趣小组设计如图微型实验装置.实验时,先断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表A指针偏转.
某兴趣小组设计如图微型实验装置.实验时,先断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表A指针偏转.(1)断开K2,闭合K1时,直流电源
(2)断开K1,闭合K2时,铜电极上的电极反应式为:
导线中电流从
(3)氯碱工业电解的饱和食盐水需要精制,为去除盐水中的Ca2+、Mg2+、Fe3+、SO42-,
提供的试剂有①Na2CO3溶液 ②BaCl2溶液 ③NaOH溶液 ④HCl,则加入试剂的正确顺序是
考点:电解原理
专题:电化学专题
分析:(1)实验时,断开K2,闭合K1,装置是电解池,石墨作阳极,铜是阴极,阳极上氯离子放电生成氯气,阴极上氢离子放电生成氢气,所以两极均有气泡产生;
(2)一段时间后,断开K1,闭合K2,形成氢氯燃料电池,铜作负极氢气失电子发生氧化反应,石墨作正极;电流从正极流向负极,溶液中阴离子向负极移动;
(3)根据除去钙离子用碳酸根离子进行沉淀,除去镁离子用氢氧根离子进行沉淀,除去硫酸根离子用钡离子沉淀,过量的钡离子需要用碳酸根离子除去,加入盐酸可以除去过量的碳酸钠和氢氧化钠等进行分析.
(2)一段时间后,断开K1,闭合K2,形成氢氯燃料电池,铜作负极氢气失电子发生氧化反应,石墨作正极;电流从正极流向负极,溶液中阴离子向负极移动;
(3)根据除去钙离子用碳酸根离子进行沉淀,除去镁离子用氢氧根离子进行沉淀,除去硫酸根离子用钡离子沉淀,过量的钡离子需要用碳酸根离子除去,加入盐酸可以除去过量的碳酸钠和氢氧化钠等进行分析.
解答:
解:(1)实验时,断开K2,闭合K1,装置是电解池,石墨作阳极,铜是阴极,阳极上氯离子放电生成氯气,阴极上氢离子放电生成氢气,所以两极均有气泡产生
;石墨为阳极,则与石墨相连的为原电池的正极,即A为正极;溶液为饱和食盐水,则电解的离子方程式为:2Cl-+2H2O
2OH-+H2↑+Cl2↑;铜是阴极,阴极上氢离子得电子生成氢气,同时阴极附近还生成氢氧根离子,所以阴极即铜电极附近滴加酚酞呈红色;
故答案为:A;2Cl-+2H2O
2OH-+H2↑+Cl2↑;铜;
(2)一段时间后,断开K1,闭合K2,形成氢氯燃料电池,铜作负极氢气失电子发生氧化反应,其电极上的电极反应式为:H2-2e-=2H+,电流从正极流向负极,即从石墨电极流向铜电极,溶液中阴离子向负极移动,则溶液中阴离子朝铜电极方向移动;
故答案为:H2-2e-=2H+;石墨,铜,铜;
(3)先加入足量的③NaOH,除去镁离子;然后加入过量②BaCl2,除去SO42-、CO32-;再加入过量①Na2CO3 除去Ca2+和过量的钡离子,过滤后,滤液中加入过量的④盐酸,除去溶液中剩余的碳酸根和氢氧化钠中的氢氧根,最后加热除去剩余的氯化氢,③②可以互换,故合理顺序是:③②①④或②③①④,
故答案为:③②①④.
;石墨为阳极,则与石墨相连的为原电池的正极,即A为正极;溶液为饱和食盐水,则电解的离子方程式为:2Cl-+2H2O
| ||
故答案为:A;2Cl-+2H2O
| ||
(2)一段时间后,断开K1,闭合K2,形成氢氯燃料电池,铜作负极氢气失电子发生氧化反应,其电极上的电极反应式为:H2-2e-=2H+,电流从正极流向负极,即从石墨电极流向铜电极,溶液中阴离子向负极移动,则溶液中阴离子朝铜电极方向移动;
故答案为:H2-2e-=2H+;石墨,铜,铜;
(3)先加入足量的③NaOH,除去镁离子;然后加入过量②BaCl2,除去SO42-、CO32-;再加入过量①Na2CO3 除去Ca2+和过量的钡离子,过滤后,滤液中加入过量的④盐酸,除去溶液中剩余的碳酸根和氢氧化钠中的氢氧根,最后加热除去剩余的氯化氢,③②可以互换,故合理顺序是:③②①④或②③①④,
故答案为:③②①④.
点评:本题综合考查电解池和原电池知识、物质的分离提纯,注意把握电化学工作原理,为高考常见题型,侧重于学生的分析能力的考查,难度中等.

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目
下列是某学生自己总结的一些规律,其中正确的是( )
| A、有的无机化学反应不属于化合、分解、置换、复分解中的任何一种反应 |
| B、某物质在固态时能导电,可确认该物质是金属单质 |
| C、一种元素在同一物质中可显示不同价态,但一定是该元素的相邻价态 |
| D、氧化物只可能是氧化产物,不可能是还原产物 |
在相同温度下,在体积相同的两个密闭容器内充入等质量的CO2和SO2气体,则下列说法正确的是( )
| A、CO2和SO2中物质的量比为1:1 |
| B、CO2和SO2的密度比为1:1 |
| C、CO2和SO2的物质的量浓度比为11:16 |
| D、CO2和SO2中所含氧原子个数比为16:11 |
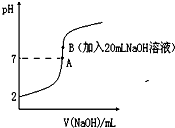 氢氟酸(HF)是一元弱酸,在水溶液中的电离方程式为:HF?H++F-.25℃下,向20mL0.2mol?L-1的氢氟酸中滴加0.2mol?L-1的NaOH溶液时,溶液的pH变化如图所示.
氢氟酸(HF)是一元弱酸,在水溶液中的电离方程式为:HF?H++F-.25℃下,向20mL0.2mol?L-1的氢氟酸中滴加0.2mol?L-1的NaOH溶液时,溶液的pH变化如图所示.