题目内容
(l4分)(1)①常温下,0.01mol/L的二元酸H2A溶液的pH=5,其电离方程式为________。
②用Al2(SO4)3与NaHCO3溶液混合反应就是泡沫灭火器的工作原理,请写出反应的离子方程式________________________________________________________。
③ 比较0.1mol/L的下列各种溶液的pH大小:
CH3COONa___________NaClO;CuSO4_________KHCO3。(填“>”、“<”或“=”)
(2) 25℃时,如果取0.1mol/LHA溶液与0.1mol/LNaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=10。试回答以下问题:
①混合溶液中由水电离出的c(H+)________0.1mol/LNaOH溶液中由水电离出的c(H+);(填“>”、“<”、或“=”)
②求出混合物中下列算式的计算结果(填具体数字):
c(A-)+c(HA)= mol/L; c(OH-)-c(HA)= mol/L。
【答案】
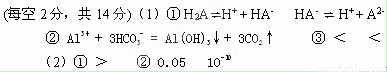
【解析】略

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目

 2(SO4)3与NaHCO3溶液混合反应就是泡沫灭火器的工作原理,请写出反应的离子方程式________________________________________________________。
2(SO4)3与NaHCO3溶液混合反应就是泡沫灭火器的工作原理,请写出反应的离子方程式________________________________________________________。  字):
字):